多発性腫瘍症候群
フェレットにおいて、リンパ腫は、臨床上遭遇する最も重要な腫瘍性疾患の一つで、全腫瘍の発生率においてもインスリノーマおよび副腎皮質新生物に次いで3番目に多いと報告されています〔Erdman et al.2008〕。また、フェレットの腫瘍学における最大の臨床的課題は、これらの新生物が単独で発生するとは限らない点にあります。特に高齢の個体では、リンパ腫がインスリノーマや副腎疾患といった他の内分泌系新生物と同時に発生しているケースが極めて一般的です。実際、リンパ腫のフェレットが副腎疾患やインスリノーマを併発していた事例は珍しくはありません。これらの腫瘍の併発は、診断と治療における深刻なジレンマを生じさせます。インスリノーマや炎症性腸疾患の一般的な管理には、プレドニゾンなどのグルココルチコイドが頻繁に使用されます 。しかし、リンパ球はグルココルチコイドに対して高い感受性を持つため、これらの基礎疾患に対する治療が、併発している未診断のリンパ腫の症状を一時的に隠蔽し、診断を著しく困難にする可能性があります〔Ammersbach et al.2008〕。さらに重大なのは、先行するステロイドの使用が、その後の化学療法プロトコールの根幹を成す薬剤(プレドニゾンを含む)に対する多剤耐性を誘導する危険性があることです 。これにより、将来的な治療の選択肢と効果が著しく損なわれる可能性があります。したがって、フェレットのリンパ腫を理解する上では、この多発性腫瘍症候群という特有の文脈を常に念頭に置く必要があります。
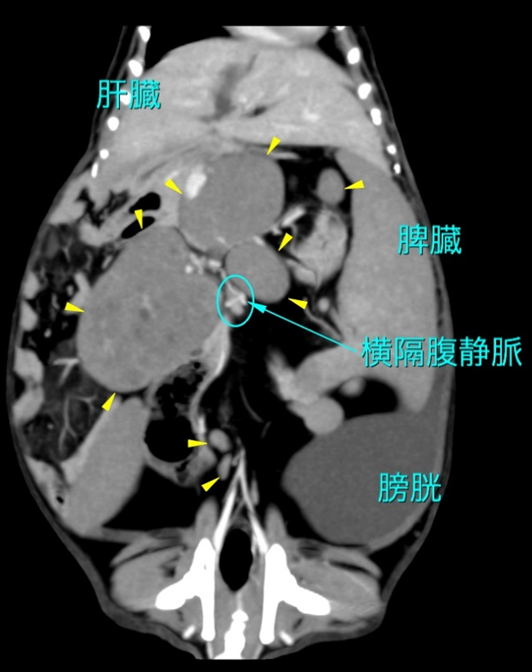
発生
腫瘍の発生率は年齢と共に上昇し、特に4.5歳から9歳に好発します。
病因
フェレットのリンパ腫の発生機序に関して、確定的な単一の病因は特定されていません 。環境要因や遺伝的素因の関与が示唆されていますが、その詳細は不明なままです。 長年にわたり、イヌ、ネコ、ウシにおけるリンパ腫と同様に 、フェレットにおいてもレトロウイルスによる病因が仮定されてきました。この仮説の状況証拠として、飼育施設や一般家庭内でのリンパ腫のクラスター発生が複数報告されていること、さらに細胞または細胞を含まない接種物による水平伝播が実験的に示されたこと が挙げられます。しかし、この仮説を裏付ける決定的な証拠は得られていません。既知の関連ウイルス、特にネコ白血病ウイルスやアリューシャン病ウイルとの関連性は、血清学的および病理学的研究によって明確に否定されています 。今日に至るまで、原因となる特異的なウイルス因子は同定されておらず、もしウイルスが関与しているとすれば、それは未だ発見されていないフェレット特有の病原体である可能性が残されています〔Williams et al.2020,Erdman et al.1992〕。 全身性のリンパ腫とは異なる病態として、胃の粘膜関連リンパ組織リンパ腫の存在が報告されています。この病型は、フェレットの胃に常在する細菌であるHelicobacter mustelaeの慢性感染と強く関連していることが示唆されています〔Williams et al.2020〕。
分類
フェレットのリンパ腫の予後を正確に予測し、適切な治療法を選択するためには、単一の分類ではなく、複数のシステム(解剖学的位置、組織学的グレード、免疫表現型)を組み合わせた多角的な評価が不可欠です。
年齢別分類
伝統的にフェレットのリンパ腫は発症年齢に基づいて2つの主要な形態に分類されてきました〔Hoppes 2010〕 。
若齢型
2歳未満での発生。急性の経過、縦隔腫瘤(胸腺)の形成、高グレードのリンパ芽球性細胞、末梢血リンパ球増多を特徴とするとされていました 。
成体型
3歳以上での発生。慢性の経過、腹腔内臓器(腸間膜リンパ節、肝臓、脾臓)または多中心性の浸潤、リンパ球減少、低グレードの細胞を特徴とするとされていました。
しかし、近年の複数の研究により、この厳格な年齢二分法はもはや臨床的に信頼できないことが示されています。かつては若齢型に限定されると考えられていたリンパ芽球性(高グレード)のリンパ腫が、あらゆる年齢のフェレットで確認されており、全体として末梢リンパ節腫脹やリンパ球増多症はむしろまれな所見であることも報告されています 。
解剖学的分類
発生部位による分類は、臨床症状と予後を予測する上で依然として重要です。
多中心型
最も一般的な形態の一つ。複数のリンパ節、脾臓、肝臓など、全身のリンパ系臓器が侵されます 。
縦隔型
胸腺および縦隔リンパ節が侵されます。古典的な若齢型と関連付けられてきましたが、どの年齢でも起こり得ます。胸水の貯留とそれに伴う呼吸困難を引き起こすことが多いです 。
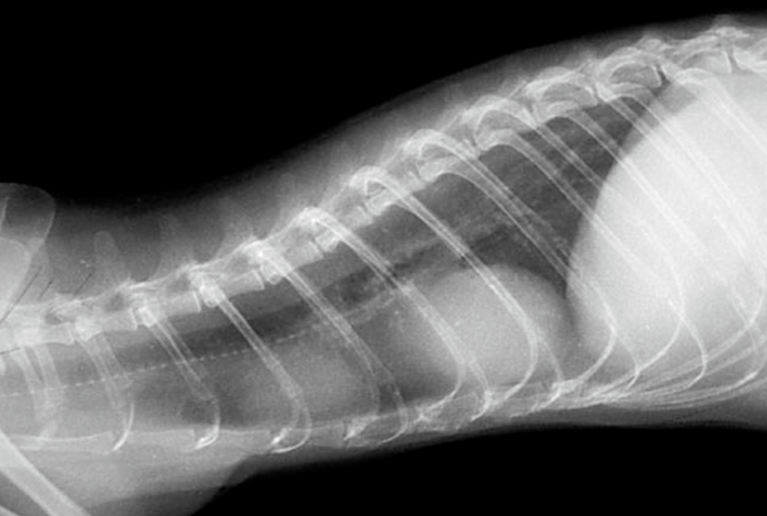
消化器型
胃、腸管、および関連する腸間膜リンパ節が侵されます。Helicobacter関連のMALTリンパ腫から、予後不良の高グレードリンパ腫まで、多様な病態を含みます。

皮膚型
皮膚および皮下組織に発生します。まれですが、皮膚向性T細胞リンパ腫(Epitheliotropic T-cell Lymphoma、菌状息肉症)などが知られています 。
節外型
リンパ系以外の単一臓器が主座となるものです。眼、中枢神経系、腎臓、心臓、骨など、あらゆる臓器が発生部位となり得ます 。
組織学的分類
腫瘍細胞の形態(細胞の大きさ、核分裂像の数)に基づいて悪性度(グレード)を分類します。イヌ、ネコ、ヒトで用いられるWHO(世界保健機関)分類やNCI(米国国立癌研究所)ワーキング分類の基準が応用されています 。
低グレード〔高分化〕
主に小型の成熟したリンパ球から構成されます(例:びまん性小リンパ球性)。一般的に進行は緩やかです。
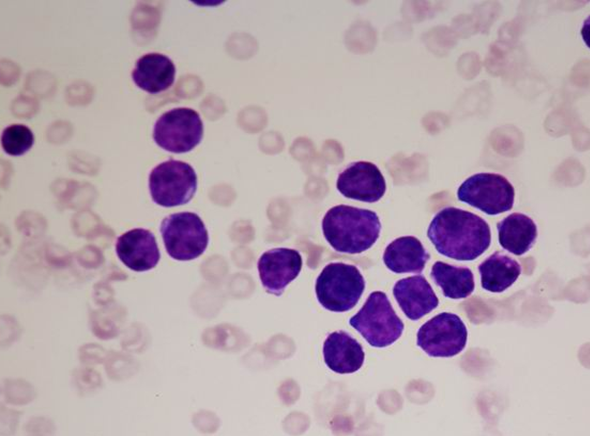
高グレード〔低分化〕
中型から大型の未成熟なリンパ球から構成されます(例:リンパ芽球性)。進行が速く、侵襲性が高い病態です。
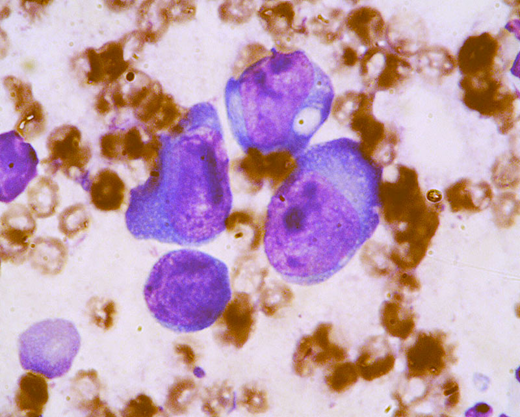
免疫表現型分類
腫瘍細胞の由来(T細胞性かB細胞性か)を特定する分類であり、最も重要な予後因子の一つです 。
T細胞性リンパ腫: 末梢性T細胞リンパ腫や未分化大細胞T細胞リンパ腫など 。
B細胞性リンパ腫: びまん性大細胞型B細胞リンパ腫や未分化大細胞B細胞リンパ腫など 。
疫学的に、フェレットのリンパ腫は、イヌ(一般にB細胞性が多い)とは異なり、T細胞性リンパ腫の発生率が有意に高いことが報告されています 。Ammersbachらによる研究では、29例中22例(76%)がT細胞性であり、B細胞性は5例(17%)でした。このT細胞優位の傾向は、フェレットのリンパ腫の全体的な予後を規定する重要な要素となっています〔Ammersbach et al.2008〕。
特殊な病型:ホジキン様リンパ腫
まれですが、フェレットにおいてもホジキン様リンパ腫が報告されています 。ヒトのホジキンリンパ腫に特徴的なリード・ステルンベルグ様細胞の出現を特徴とし 、診断には厳密な病理組織学的評価と免疫染色が必要です〔Matsumoto et al.2017〕。
症状
フェレットのリンパ腫の臨床症状は、極めて非特異的であり、浸潤している臓器によって大きく異なります。 最も一般的に認められる症状は、食欲不振、体重減少、および嗜眠(元気消失)です 。これらは、インスリノーマ、副腎疾患、IBD、心疾患など、フェレットで一般的な他の多くの消耗性疾患の症状と区別がつきません。
- 縦隔型: 胸腔内の腫瘤(多くは胸腺由来)が肺や心臓、大血管を物理的に圧迫するため、呼吸困難、努力呼吸、咳、および胸水の貯留が見られます 。
- 消化器型: 消化管壁への浸潤や腫瘤形成による閉塞により、下痢、嘔吐、黒色便(メレナ)、および顕著な体重減少が引き起こされます 。
- 皮膚型: 皮膚向性リンパ腫の場合、四肢の発赤、腫脹、脱毛、痂皮、潰瘍などが特徴的な所見となることがあります 。
- 節外型(CNS): 脊髄への浸潤は、後肢の脱力や麻痺を引き起こすことがあります 。

診断・臨床病期分類(ステージング)
確定診断には、リンパ球の異常な増殖を証明するための組織サンプルの採取が不可欠です。 診断的ワークアップとして、血液検査(CBC、血液化学検査)を行い、全貌の確認のために X線検査(特に胸部、縦隔腫瘤や胸水の評価)および腹部超音波検査(腹腔内リンパ節、肝臓、脾臓、消化管の評価)が必須です 。超音波検査は、細胞診や生検のためのサンプル採取のガイドとしても極めて有用です 。さらなる詳細にはCTやMRIも有用です。
確定診断
細胞診検査は低侵襲であり、鎮静下または無麻酔で実施可能です。高グレードのリンパ芽球性リンパ腫の場合、均一なリンパ芽球集団が認められ、診断的な場合がありますが、信頼性に欠けることが多く 、特にフェレットのサンプル評価に精通した病理医による評価が不可欠です 。低グレードリンパ腫と反応性過形成(炎症などによる)との鑑別は、細胞診のみでは極めて困難か、しばしば不可能です。したがって最終的な確定診断は組織生検がゴールドスタンダードです 。外科的(切除生検)または内視鏡、超音波ガイド下(針生検)で組織を採取します。 組織生検は、単なるリンパ腫であるという診断を超えて、組織構造の評価を可能にし、予後と治療法を決定するために不可欠な組織学的グレードおよび免疫表現型の分類を可能にする唯一の方法になります。 組織生検サンプルを用いて、細胞表面マーカーを染色します。フェレットではT細胞マーカー(CD3)とB細胞マーカー(CD79α)のパネルが、フェノタイプを決定するために最も重要です〔Hammer et al.2007〕。
臨床病期分類(クリニカル・ステージング)
腫瘍の全身への広がりを定義するために、すべての症例でステージングを行う必要があります 。イヌやネコで用いられるWHOの5段階ステージングシステムが最も一般的に推奨されます 。
| ステージ | 定義 |
| ステージ I | 単一のリンパ節、または単一の節外臓器(リンパ節の関与なし)の浸潤 |
| ステージ II | 横隔膜の片側(同側)にある複数のリンパ節の転移 |
| ステージ III | 横隔膜の両側にある複数の(全身性)リンパ節の転移。 |
| ステージ IV | 肝臓および/または脾臓の浸潤(リンパ節の関与の有無を問わない) |
| ステージ V | 血液(白血病)または骨髄、および/または他の臓器(CNS、眼、腎臓など)への浸潤 |
治療
フェレットのリンパ腫治療は、多くの場合、治癒を目指すものではなく、寛解導入と生活の質(QOL)の維持を目的とします 。治療の選択は、上記で確立されたステージ、グレード、フェノタイプ、および併発疾患の有無に基づいて決定されます。
外科的治療
外科手術が根治的治療となるのは、ステージIの孤立性腫瘍(例:皮膚型リンパ腫の単一病変、単一リンパ節のホジキン様リンパ腫)に限られます。 ほとんどの場合、リンパ腫は診断時点で全身性の疾患(ステージIII以上)です。そのため、外科手術は診断のための生検サンプル採取 、またはQOL改善のための姑息的な減量術(例:閉塞を引き起こす消化管腫瘤、不快感を伴う巨大な脾臓の摘出)として行われます〔Williams et al.2020〕 。
放射線治療
リンパ腫は一般的に放射線感受性が高い腫瘍です。 放射線治療は、化学療法と組み合わせた集学的治療の一部として、または化学療法に抵抗性となった場合の救済治療(レスキュー)として用いられます。呼吸困難を引き起こしている縦隔型腫瘤の緊急的な縮小(姑息的治療)、または局所的な節外性病変(例:CNS、骨)の制御に有効な場合があります。Hutsonら は、ドキソルビシンとオルソボルテージ放射線療法を組み合わせた救済治療を報告しています〔Hutson et al.1992〕。 しかし、フェレットにおける特化したプロトコール(総線量や分割照射法)は標準化されておらず 、実施可能な施設は限られます。
緩和治療(プレドニゾン単剤療法)
プレドニゾン(またはプレドニゾロン)単剤での経口投与は、安価で侵襲性が低いため、広く用いられている治療法です 。投与量としては、1~2mg/kg sidなど、様々な用量が報告されています。 プレドニゾンはそのリンパ球溶解作用により、高グレードリンパ腫に対し、短期間(約1ヶ月程度)の症状改善(食欲増進など)と腫瘍縮小をもたらすことがあります〔Williams 2017〕 。しかし、この効果は一時的であり、腫瘍細胞はすぐに抵抗性を獲得し再燃します。複数の研究および総説が、プレドニゾン単剤治療は、治療しない場合と比較して、生存期間中央値(MST)を有意に延長しない可能性が高いという意見も多いです。最も重要な懸念は、プレドニゾンへの曝露がP糖タンパク質を介した多剤耐性(MDR)を誘導し、その後に実施するであろう多剤併用化学療法(COP/CHOPなど)の効果を著しく減弱させるリスクがあることです。 プレドニゾン単剤療法は、もはや「治療」とは見なされず、積極的な化学療法を飼い主が拒否した場合の「ホスピス・ケア」またはQOLの短期的な改善を目的とした姑息的手段としてのみ位置づけられるべきです。
化学療法プロトコール
全身性疾患であるリンパ腫の治療の主体は、多剤併用化学療法です 。フェレットのプロトコールは、その多くがイヌとネコのプロトコールを改変したものです 。 免疫表現型と組織学的分類の分類によって治療方向性が以下の表のように決定できます。
| 分化 | 免疫表現 | 予後 | 治療 |
| 低グレード(高分化) | B細胞 | 軽めの治療で長期生存可 | プレドニゾロン+ クロラムブシル |
| T細胞 | 抗癌剤の反応不良だが, 長期生存可 | ||
| 高グレード(低分化) | B細胞 | 抗癌剤の反応良好 | 多剤併用抗癌剤 |
| T細胞 | 抗癌剤の反応不良 | 多剤併用抗癌剤 |
低グレード・小細胞性リンパ腫の治療
適応: 組織学的に「低グレード」または「小リンパ球性」と診断された症例(特に高齢フェレットの慢性経過の消化器型や多中心型)。
治療戦略(ネコからの外挿): フェレットに特化した低グレードリンパ腫の確立された研究は少ないですが、ネコの小細胞性消化器型リンパ腫で非常に良好な結果(MST 1000日以上)が報告されているプレドニゾンとクロラムブシルの併用経口プロトコール〔Pope et al.2015〕が、第一選択として考慮されます 。高グレード型に用いられるアグレッシブなプロトコールは、低グレードリンパ腫には過剰な毒性をもたらす可能性があるため、治療の層別化が重要です。
高グレード・多中心型リンパ腫(CHOP/COPベース)
原理: 高グレード(リンパ芽球性、大細胞性)リンパ腫に対する標準治療です。作用機序の異なる複数の薬剤を組み合わせることで、相乗効果を高め、耐性の出現を遅らせます。
臨床的有効性: CHOPまたはCOP(ドキソルビシンを含まない)をベースとした多剤併用プロトコール(IV投与を含む)で治療されたフェレットの生存期間中央値(MST)は429日(約14ヶ月)であったとする報告があり〔Webb et al.2019〕 、プレドニゾン単剤や無治療の予後(平均6ヶ月 )を大幅に改善する可能性があります。
1989年には既に、Duganらが〔Dugan et al.1989〕、Cotter〔Cotter 1983〕とMacEwanら〔MacEwan et al.1987〕から引用した犬の治療レジメンの様々な側面から派生したプロトコルを用いて、フェレットの多中心性リンパ腫の化学療法による寛解を報告しました。この症例報告では、L-アスパラギナーゼ、経口プレドニゾロン、経口シクロホスファミドを用いることで、21週間の化学療法後にX線画像と超音波画像による評価で完全寛解が得られたことが示されました.
| 週 | 薬剤 | 投薬量 |
| 1 | Lアスパラギナーゼ | 400IU/kg IP |
| プレドニゾロン | 1.6mg/kg PO SID | |
| 2 | シクロホスファミド | 336mg/m2 PO 4日間に分けて |
| プレドニゾロン | 1.6mg/kg PO SID | |
| 3 | Lアスパラギナーゼ | 400IU/kg IP |
| プレドニゾロン | 1.6mg/kg PO SID | |
| 4、6、9、11、13 | シクロホスファミド | 252mg/m2 PO 3日間に分けて |
| プレドニゾロン | 1.6mg/kg PO SID | |
| 17、20、23、26その後 3週毎、再発するまで | シクロホスファミド | 168mg/m2 PO 2日間に分けて |
| プレドニゾロン | 1.6mg/kg PO SID 36週まで |
1993年、Brownは、ニューヨーク市の動物医療センターの腫瘍専門医がフェレットの化学療法プロトコルを用いて成功を収めたと報告しました〔Brown 1993〕。
| 週 | 薬剤 | 投薬量 |
| 1 | ビンクリスチン | 0.07mg/kg IV |
| 2 | シクロホスファミド | 10mg/kg PO |
| 3 | ビンクリスチン | 0.07mg/kg IV |
| 4 | メトトレキサート | 0.5mg/kg SC |
| 5 | ビンクリスチン | 0.07mg/kg IV |
| 6 | シクロホスファミド | 10mg/kg PO |
| 7 | ビンクリスチン | 0.07mg/kg IV |
| 8 | メトトレキサート | 0.5mg/kg SC |
1年後、Rosenthalは、リンパ肉腫の犬について発表されたものと非常によく似た別の化学療法プロトコルを報告しました〔Rosenthal 1994〕。
| 週 | 薬剤名 | 投与量 |
| 1 | ビンクリスチン | 0.07mg/kg IV |
| Lアスパラギナーゼ | 400IU/kg IP | |
| プレドニゾン | 1mg/kg PO SID | |
| 2 | シクロホスファミド | 10mg/kg SC |
| プレドニゾン | 1mg/kg PO SID | |
| 3 | ドキソルビシン | 1mg/kg IV |
| プレドニゾン | 1mg/kg PO SID | |
| 4-6 | 1-3週の薬剤を繰り返して投与(Lアスパラギナーゼは除く) | |
| 8 | ビンクリスチン | 0.07mg/kg IV |
| プレドニゾン | 1mg/kg PO SID | |
| 10 | シクロホスファミド | 10mg/kg SC |
| プレドニゾン | 1mg/kg PO SID | |
| 12 | ビンクリスチン | 0.07mg/kg IV |
| プレドニゾン | 1mg/kg PO SID | |
| 14 | メトトレキサート | 0.5mg/kg IV |
| プレドニゾン | 1mg/kg PO SID | |
また、2000年にはAntinoff(私信、2003年8月)が、ヒューストンのGulf Coast Veterinary Specialistsの腫瘍専門医の推奨に基づき、フェレットの悪性リンパ腫の治療に効果的に用いられているCOP-Lプロトコルについて報告しました。さらに、ブラウンは、ドキソルビシン1mg/kgを21日ごとに静脈内投与し、最大5回の治療を行うことを、単剤化学療法または、別のプロトコルで寛解した後に疾患が再発した患者に対する救済療法として説明しています。
| 週 | 薬剤名 | 投薬量 |
| 3日 | Lアスパラギナーゼ | 400IU/kg IP |
| 1 | ビンクリスチン | 0.10mg/kg IV |
| プレドニゾン | 1mg/kg PO SID 治療期間中継続 | |
| シクロフォスファミド | 10mg/kg PO ビンクリスチン投与24時間後投与 | |
| 2 | ビンクリスチン | 0.10mg/kg IV |
| 3 | ビンクリスチン | 0.10mg/kg IV |
| 4 | ビンクリスチン | 0.10mg/kg IV |
| シクロフォスファミド | 10mg/kg PO ビンクリスチン投与24時間後投与 | |
| 7 | ビンクリスチン | 0.10mg/kg IV |
2003年、マイヤーらは、タフツ大学獣医学部で開発された、フェレットリンパ腫に対する新しい化学療法プロトコルを発表しました。このプロトコルでは、経口または皮下投与のみで薬剤を投与し、静脈穿刺や外科手術の必要性を完全に排除しています。プレドニゾン、L-アスパラギナーゼ、シクロホスファミド、シタラビン、メトトレキサート、クロラムブシル、プロカルバジンが使用されます。このプロトコル全体は27週間にわたり、その間に19回の治療が必要です.しかし、このプロトコールで治療されたフェレット7例のMSTは86日であったという報告があります 。〔Mayer et al.2003〕。これに対し、前述のIVを含むCOPベースのプロトコール群のMSTは429日でした 。このデータは、両群の背景(グレードやステージ)が制御されていない限定的なものであり、直接比較は困難ですが、利便性(No-IV)を追求したプロトコールが、より標準的でアグレッシブなIVプロトコールと比較して、生存期間において劣る可能性を示唆しています。この潜在的な有効性のトレードオフは、飼い主とのインフォームド・コンセントにおいて極めて重要な議論となります。
| 週 | 薬剤 | 投薬量 |
| (継続) | プレドニゾン | 2mg/kg PO SID (7日間), その後 q48h で継続 |
| 1 | Lアスパラギナーゼ | 10,000 IU/m2 SC |
| シクロホスファミド | 250mg/2 PO (50mL/kg LRSと共に) | |
| 2 | Lアスパラギナーゼ | 10,000IU/m2 SC |
| 3 | Lアスパラギナーゼ | 10,000IU/m2 SC |
| シタラビン | 300mg/m2 SC SID (2日間) | |
| 5 | シクロホスファミド | 250mg/ⅿ2 PO (50mL/kg LRSと共に) |
| 7 | メトトキシレート | 0.8mg/kg IM |
| 9 | シクロホスファミド | 250mg/m2 PO (50mL/kg LRSと共に) |
| 11 | シタラビン | 300mg/m2 SC SID (2日間) |
| クロラムブシル | 1mg PO SID (2日間) | |
| 13 | シクロホスファミド | 250mg/ⅿ2 PO (50mL/kg LRSと共に) |
| 15 | プロカルバジン | 50mg/m2 PO SID (14日間) |
| 18 | シクロホスファミド | 250mgⅿ/2 PO (50mL/kg LRSと共に) |
| 20 | シタラビン | 300mg/m2 SC SID (2日間) |
| クロラムブシル | 1mg PO SID (2日間) | |
| 23 | シクロホスファミド | 250mg/2 PO (50mL/kg LRSと共に) |
| 26 | プロカルバジン | 50mg/m2 PO SID (14日間) |
| モニタリング | CBC | Week 2, 4, 8, 12, 16, 17, 27 |
化学療法の毒性と副作用管理
ヒトやイヌの化学療法で一般的に見られる重度の悪心、嘔吐、消化器症状、および顕著な脱毛は、フェレットではまれです 。これは、QOL維持の観点から飼い主にとって非常に重要な情報です。食欲不振や嘔吐、シミンが見られることはあります。 フェレットにおける化学療法の最も重要な用量規制毒性です。特にシクロホスファミドやビンクリスチンは、重度の好中球減少症を引き起こす可能性があります 。すべての骨髄抑制性のある薬剤の投与前には、必ずCBC(全血球計算)を実施し、好中球数をモニタリングする必要があります。 好中球数が一定の閾値(例:1,000-1,500/μL)を下回った場合、その週の投与は延期し、次回の投与量を25%減量するなどの調整が必要です。好中球数が1,000/μL未満に低下した場合、発熱がなくとも敗血症のリスクが高まるため、予防的な広域抗生物質の投与が推奨されます 。ヒトやイヌでは 、重度の好中球減少症の期間を短縮するために、G-CSF(顆粒球コロニー刺激因子)が使用されます。フェレットでのエビデンスは乏しいですが、有用である可能性が示唆されています 。 シクロホスファミドによる無菌性出血性膀胱炎(LRSの同時投与で予防)、ドキソルビシンによる累積性心毒性(総投与量に注意)など、薬剤特異的な毒性にも注意が必要です。
参考文献
- Ammersbach M et al.Laboratory findings,histopathology,and immunophenotype of lymphoma in domestic ferrets.Vet Pathol45(5):663-73.2008
- Brown S.Lymphoma,ferrets.Proc North Am Vet Conf:730-732,1993
- Cotter SM.Treatment of lymphoma and leukemia with cyclophosphamide,vincristine,and prednisone:Treatment of
dogs.JAAHA19:159-163.1983 - Dugan SJ,Center SA,Randolph JF,Anderson WT.Chemotherapeutical remission of multicentric lymphosarcoma in a ferret
(Mustela putorius furo). AAHA25:69-74.1989 - Erdman SE,Moore FM,Rose R,Fox JG.Malignant lymphoma in ferrets:clinical and pathological findings in 19 cases.J Comp Pathol;106(1):37-47.1992
- Erdman SE,Brown SA,Kawasaki TA,Moore FM,Li X,Fox JG.Clinical and pathologic findings in ferrets with lymphoma:60 cases (1982-1994).J Am Vet Med Assoc15;208(8):1285-1289.1996
- Hammer AS et al.High-throughput immunophenotyping of 43 ferret lymphomas using tissue microarray technology.Vet Pathol44(2):196-203.2007
- Hutson CA,Kopit MJ,Walder EJ.Combination doxorubicin and orthovoltage radiation therapy,single-agent doxorubicin,and high-dose vincristine for salvage therapy of ferret lymphosarcoma.J Am Anim Hosp Assoc28:365-368.1992
- Hoppes SM.The Senior Ferret (Mustela Putorius Furo).Vet Clin North Am Exot Anim Pract11;13(1):107-122.2010
- MacEwan EG,Hayes AA,Matus RE,Kurzman I.Evaluation of some prognostic factors for advanced multicentric lymphosarcoma in the dog:147 cases (1978–1981).JAVMA190(5):564-568.1987
- Matsumoto I et al.Hodgkin’s-like lymphoma in a ferret (Mustela putorius furo).J Vet Med Sci11;79(10):1660–1663.2017
- Mayer J,Payne S,Mateleska J,Moore AS:A novel chemotherapy protocol for lymphoma in ferrets.Proc Br Vet Zoo Soc Spring
Meeting,Dublin,Ireland,May 9-11.2003 - Pope KV et al.Outcome and toxicity assessment of feline small cell lymphoma: 56 cases (2000–2010).Vet Med Sci29;1(2):51-62.2015
- Rosenthal K.Ferrets,in Veterinary Clinics of North America,Exotic Pet Medicine II.WB Saunders.Philadelphia:p19-20.1994
- Webb JK et al.Presentation and survival time of domestic ferrets(Mustela putorius furo) with lymphoma treated with single- and multi-agent protocols:44 cases (1998-2016).ournal of Exotic Pet Medicine31.2019
- Williams BH,Wyre NR.Neoplasia in Ferrets.Ferrets,Rabbits,and Rodents29:92-108.2020
- Williams BH.Therapeutics in Ferrets.Vet Clin North Am Exot Anim Pract26;3(1):131-153.2017

