無麻酔保定
CT画像の質は、被写体の不動化にかかっています。爬虫類の保定法は、検査の目的、個体の気質、および健康状態に応じて、物理的保定から全身麻酔まで段階的に選択されます。しかし、爬虫類は動作が緩慢な場合が多く、適切な物理的保定を行えば無麻酔での撮影が可能です。これは麻酔リスクを回避できる点で有利になります。
カメ
四肢と頭部を甲羅内に収納させ、粘着テープを用いて甲羅の上から、頭、四肢、尾を押し込んだ状態にすることで、不意な体動を防ぐことができます。また、紙やプラスチック容器に入れることで、ガントリーからの落下を防げます。
原則として腹位で撮影します。仰臥位(背位)にすると内臓(特に肺に対する消化管の圧迫)の位置関係が不自然になり、生理的な評価が困難になるためです。本来は可能な限り四肢を甲羅の外に出して撮影することが理想的ですが(肺野との重なりを避けるため)、CTでは断層像により分離可能であるため、無理に引っ張り出す必要はありません。むしろ、四肢を甲羅内に収納してテーピング固定する方が、体動抑制の観点からは確実でしょう。
大型のカメでは身体に適した大きさの容器に入れることで、意外に大人しく撮影することができます。
ヘビ
アクリル製や塩化ビニル製の透明なチューブに誘導することで、直進状態を維持したまま撮影が可能です。原則として腹位撮影します。また、攻撃的でない個体であれば、発泡スチロール箱や洗濯ネットに入れ、自然にとぐろを巻いた状態で撮影することも一般的です。直進状態で撮影することで、解剖学的な位置関係(頭側から尾側への臓器配列)が保たれるため、臓器の同定が容易になります。左右の肺(あるいは発達した右肺と退化した左肺)の対称性や、気管・肺の走行を連続的に追跡しやすいです。しかし、全長が長い個体(ニシキヘビなど)では、CTの最大スキャン範囲(Scan length)を超える可能性があり、また管への導入自体が動物にストレスを与える場合があります。

しかし、管のサイズにヘビの全長が適するとは限りません。管の中での隙間が生じることで、ヘビが動いてしまうことが多いです。

大人しい個体や小さいヘビでは、直進状態で台にテープではりつける方法をとることがあります。

直進状態での撮影では、いずれの撮影腫大においても、身体の全領域が不動化した状態とは限らず、頭部、胴体全部、胴体後部と目的の部分だけを抽出して検査することもあります。
とぐろ状態での撮影は保定が容易であり、動物へのストレスが最小限で済み、つまりポジショニングに要する時間が短く、迅速な検査が可能になります。しかし、画像上の問題が非常に多くなります。重力勾配が起、つまり とぐろを巻いた状態では、体の下側になった肺領域が、上にある体節の重みで圧迫され、CT値が上昇することが報告されています(圧迫性無気肺に類似した変化)。これを肺炎による浸潤像と誤認しないよう注意が必要です〔Hedley et al.2014〕。最新のワークステーションでは、とぐろを巻いた状態のデータに対し、Curved MPR(曲線多断面再構成)を適用することで、仮想的にヘビを真っ直ぐに伸ばした画像を再構成することが可能となっています〔Hedley et al.2014〕。これにより、保定の簡便さと診断の正確さを両立できますが、画僧診断においてはやはり直進状態で撮影する方法が、臓器実質の診断においては正確性が高いです。臨床的には、一般的なスクリーニングや骨折、卵や胎子の有無、明らかな腫瘤の検索にはとぐろ状態での撮影が推奨され、微細な肺炎の評価や、外科手術のための厳密な解剖学的マッピングが必要な場合には、可能な限り直進状態での撮影を試みるべきです。
トカゲ
トカゲは種による体型の多様性が著しく、それに応じた配慮が必要になります。原則として腹位で撮影します。体動による画像のブレを防ぐため、保定箱に収納して、多くが無麻酔で検査が遂行できます。ヒョウモントカゲモドキやフトアゴヒゲトカゲなどの小型~中型のトカゲでは小さなプラスチックや紙の容器内に収容し、腹臥位を保ったまま撮影します。容器内にタオルなどを敷き詰めて、滑らないそして動かないように配慮します。


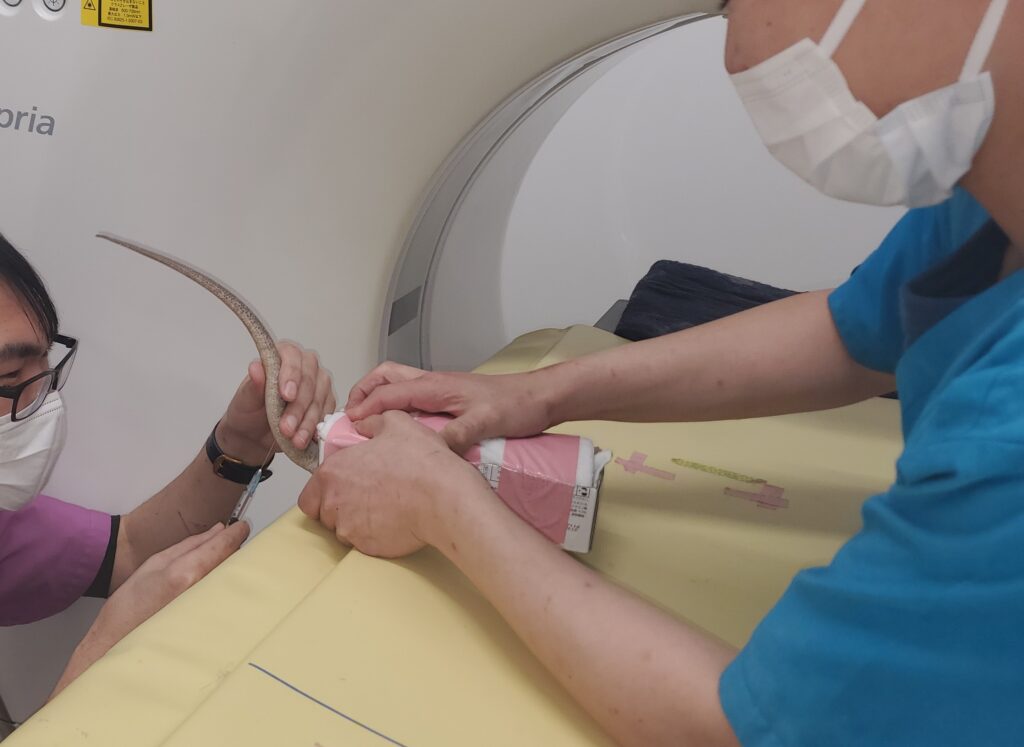
眼を濡れたガーゼで覆い軽く圧迫することで迷走神経反射を誘発し、一時的な徐脈と不動化を得る方法が、グリーンイグアナや大型モニターにおいて伝統的に用いられています 。四肢を体側に寄せてテープで台に固定する場合もあります。
脂肪体(Fat Bodies)の活用
多くのトカゲ(モニター、フトアゴヒゲトカゲ、ヒョウモントカゲモドキなど)は、腹腔内後方に一対の大きな脂肪体を持っています。脂肪組織はCT値が低く(-100 HU前後)、周囲の臓器(腎臓、腸管、生殖器)とのコントラストを明瞭にする役割を果たします〔Melero et al,2024〕。特に肥満個体では、脂肪体のおかげで、造影剤を使用せずとも臓器の輪郭が明瞭に描出される場合があります。
カメレオン
カメレオンは平らな面(床)に腹臥位で置かれるとストレスを感じ、不安定になります。多くの個体は、止まり木などの足場がある方が精神的に安定し、不動化しやすい特徴があります。自然な状態に近づけるため、木の枝(止まり木)をつかませた状態で撮影を行いますが、止まり木以外にも、タオルなどを敷いた上に腹位にさせて静置できます。しかし、実際は木の枝をつかませた状態でも動く個体が多く、鎮静あるいは麻酔が必要になります内臓の重なり、肺の圧迫を避けるために、原則として腹位で撮影します。麻酔下であればタオル等で体を支えて腹位を維持します。しかし、カメレオンの肋骨は非常に細く繊細で、過度な力で握る等の物理的保定を行うと、容易に医原性の肋骨骨折を引き起こすリスクがありますので注意してください。また、カメレオンの肺は複雑な憩室を持ち、体腔内の広範囲に広がっています。CTではこれらの正常な肺嚢胞構造と、病的病変を区別する必要がでてきます。
造影CT検査
単純CTでは、腫瘍と筋肉、あるいは腹水と腸管の区別がつかない場合が多く、正確な診断には造影CTが不可欠になりますしかし、爬虫類における造影剤の使用には、哺乳類とは異なる特別な配慮が必要です。
造影剤の種類と投与量
オムニパーク(イオヘキソール)やイオパミドールなどの非イオン性ヨード造影剤を使用します。イオン性造影剤は浸透圧が高く、副作用のリスクが高いため爬虫類には推奨されません。投与量は400〜600mgL/kg(ヨード量換算)で、これは、濃度300mgL/mLの製剤であれば約1.3〜2.0mL/kgに相当します〔Greco et al.2022〕。高用量: 腎臓や肝臓のより強い濃染を得るために、800〜1000mg/kgまで増量する報告もあります〔Divers 2001〕。しかし、後述する腎毒性のリスクを考慮し、診断に必要な最小限の量にとどめるべきです〔Erickson et al.2024〕。小型~中型の爬虫類では、0.5~2.0mL/secの速度で投与するのが一般的です〔Marcon et al.2012〕。
血管確保のアプローチ
カメでは背甲静脈、トカゲでは尾静脈を使用します。それ以外では、鎮静や麻酔が必要になったり、皮膚のカットダウンをしないとアプローチが容易にできません。かし、トカゲで大腿骨から造影剤を注入できる報告もあり〔Erickson et al.2024〕、カメの上腕骨なども選択な可能と思われます。
爬虫類における最も重要な血管解剖学的特徴の一つが、腎門脈系の存在で、体の後半部(尾部や後肢)からの静脈血が、後大静脈へ直接還流する前に、腎臓の尿細管周囲毛細血管網を経由するシステムです。 尾静脈や後肢の静脈から造影剤を投与した場合、造影剤の大部分が腎臓を通過してしまう可能性があります。腎臓を通過する時間分、大動脈への到達が遅れ、腎臓通過中に一部が排泄、あるいは希釈され、頭側の大動脈や脳血管の造影増強効果が著しく低下します。動脈相よりも先に腎臓が強く造影されてしまい、腎動脈や周囲血管の評価を妨げる可能性があります。グリーンイグアを用いた血管造影の研究では、尾部からの血液は腎門脈循環に入る傾向が強い一方、後肢からの血液は腎臓をバイパスして全身循環に入るルートも有していることが示されていますが、種や個体の水分状態によって変動します。したがって、全身性の血管造影を行う場合は。主要動脈系の評価においては、腎門脈の影響を受けない頸静脈や前肢の静脈からのアプローチが推奨されます〔Keith et al.1999〕。
スキャンタイミング
爬虫類は心拍出量が低く、循環時間が極めて遅い。犬猫の注入後15〜20秒で動脈相という常識は通用しません。また、麻酔や体温低下により、造影剤が末梢静脈から心臓、そして動脈系へ到達するまでに長い時間を要しますので、注意してください〔Divers 2001〕。現在の爬虫類のスキャンタイミングにおいては、過去の文献データに基づいた固定時間を採用する方法が最も一般的かつ現実的です。ただし、この「固定時間」は哺乳類に比べて著しく長いことに注意が必要です。犬や猫では、注入開始から10~15秒程度で動脈相が撮影されますが、爬虫類では循環時間が遅いため、これでは早すぎて造影剤が到達していない可能性が高いです。動脈相の撮影には注入開始から 20~30秒、門脈・実質相には 60~90秒以上の待機時間が必要となるケースが大半です。
種別臨床適応別推奨プロトコル詳細
アカミミガメ〔Sochorcova et al.2017〕
頸静脈から320mgL/kg (Iodixanol等)を、注入速度: 0.5 mL/secで撮影しました。動脈相は20秒後がピークで、このタイミングで大動脈(右大動脈・左大動脈)、腕頭動脈、鎖骨下動脈などの主要動脈のピーク増強が得られます。門脈・肝静脈相は60秒後がピークで、肝実質の造影効果が最大化し、肝静脈や門脈系の描出に最適でした。遅延相は180秒後がピークで、腎臓の実質評価や腫瘍のウォッシュアウト(造影剤の抜け)を評価するために用います。
海ガメ〔Smith et al.2000〕
アカウミガメ(Caretta caretta)など大型種では、循環動態が小型カメとは異なりますが、60秒後の撮影で良好な体腔内臓器と血管構造のコントラストが得られた報告があります。
グリーンイグアナ
大腿骨骨髄内投与(Intraosseous: IO) で、ヨード造影剤(Iopamidol等)を投与しました。IO投与の場合、静脈内投与(IV)よりも循環への移行にラグが生じます。注入開始から60秒後で肝実質と肝血管系のコントラストが最大化されました。この際動脈系と静脈系が同時に造影される傾向があります〔Erickson et al.2024〕。
ボアコンストリクター
固定法の場合、カメと同様に20~30秒(動脈相)、60~90秒(静脈相)を目安としますが、体長による循環時間の延長を考慮し、さらに遅らせる(例:40秒、120秒)調整が必要になる場合があります。
| 動物種 | 造影剤投与経路 | 造影剤投与量(mg/KG) | 投与速度(mL/s) | 動脈相(秒) | 静脈/門脈相(秒) | 遅延相(秒) | 備考 |
| カメ類 (Trachemys等) | 頸静脈 | 320~ 800 | 0.5~2.0 | 20 | 60 | 180 | 心大血管評価に最適 |
| トカゲ類 (イグアナ等) | 頸静脈・前肢静脈 | 300~600 | 0.5~2.0 | 15~30 | 60 | 120+ | IV確保困難時はカットダウンも検討 |
| ヘビ類 (ボア・ニシキヘビ) | 尾静脈・心臓(※) | 300~600 | 手押し/低速 | 20~40 | 60~90 | 300+ | 心臓穿刺は最終手段/尾静脈使用時は腎門脈の影響を考慮 |
イグアナの骨髄内投与
グリーンイグアナなどの大型トカゲにおいて、血管確保が困難な場合、大腿骨への骨髄内カテーテル(Intraosseous catheter: IO)留置による造影剤投与が検討されています。グリーンイグアナを用いた研究では、大腿骨へのIO投与により、静脈内投与と同等の優れた血管造影効果が得られることが示されています。しかし、 成長期の個体における骨端軟骨板の損傷や、高圧注入による骨皮質の破損、造影剤漏出のリスクがあるため、手技には熟練を要します〔Erickson et al.2024〕。
右左シャントの影響
鎮静や保定によるストレス、あるいは自発的な息こらえにより肺血管抵抗が上昇すると、静脈血(造影剤を含む)の一部が肺循環をバイパスして直接大動脈へ流れる右-左シャントが発生します。理論上、これにより造影剤の大動脈到達時間は短縮される可能性がありますが、同時に肺での酸素化を受けていない血液と混合するため、動脈血中の造影剤濃度が希釈され、CT値のピークが低下するリスクがあります〔Kik et al.2005〕。
造影剤誘発性腎症の予防
脱水状態の爬虫類や、既存の腎疾患を持つ個体にヨード造影剤を投与すると、急性尿細管壊死を引き起こし、致命的な腎不全に至るリスクがあります。十分な輸液により循環血液量を増加させ、尿細管内での造影剤濃度を低下させるとともに、排泄を促進させることが唯一確実な予防法になります。爬虫類の維持輸液量は10〜30mL/kg/日とされ、造影CTを行う場合は、検査の数時間前〜前日から維持量の倍量程度の輸液を行い、十分な水和状態を確保します。検査後も24〜48時間は輸液を継続し、造影剤の排泄をサポートするべきです。骨髄内投与を受けたグリーンイグアナの組織学的検査において、軽度の尿細管変性が認められた報告がありま。IOルートを使用する場合、腎臓への直接的な高濃度暴露が懸念されるため、特に念入りな輸液管理が求められます〔Erickson et al.2024〕。
株式会社EICでは、犬猫以外のエキゾチックアニマルのCT、MRI画像の画像診断を行っています。犬や猫以外の画像診断を行い、症例によっては治療などの症例支援も行ってます。撮影を行ったが、読影ができない場合はEICに申し込んで下さい。

待望の新刊! 爬虫類の病気百科
エキゾチックアニマル臨床の第一人者 霍野晋吉が贈る、獣医師そして飼育者、ブリーダーまで、全爬虫類関係者へ送る医学バイブル
参考文献
- Divers SJ.Diagnostic imaging of reptiles.In Practice 23(7):370.2001
- Erickson MCM et al.Intraosseous contrast administration for coelomic computed tomography angiography in green iguanas (Iguana iguana): Preliminary findings show promise as an alternative to the intravenous route.Vet Radiol Ultrasound65(6):776-785.2024
- Greco A et al.Imaging techniques in veterinary medicine. Part II: Computed tomography, magnetic resonance imaging, nuclear medicine.Eur J Radiol Open13:10:100467.2022
- Hedley J, Eatwell K,Schwarz T.Computed tomography of ball pythons(Python regius)in curled recumbency.Comparative StudyVet Radiol Ultrasound55(4):380-386.2014
- Keith G et al.Characterization of the Renal Portal System of the Common Green Iguana (Iguana iguana) by Digital Subtraction Imaging.Journal of Zoo and Wildlife Medicine30(2):p235-241.1999
- Kik MJK,Mitchell MA.Topics in medicine and surgeryReptile cardiology: A review of anatomy and physiology, diagnostic approaches, and clinical disease.Seminars in Avian and Exotic Pet Medicine14(1):52-60.2005
- Melero A et al,Computed tomography of the coelomic cavity in healthy veiled chameleons(Chamaeleo calyptratus) and panther chameleons (Furcifer pardalis).Open Vet J13(9):1071-1081.2023
- Marcon O et al.16-Multidetector computed tomography angiography in Trachemys scripta elegans.Conference: IVRA (International Veterinary Radiology Association) EAVDI (European Association Veterinary Diagnostic Imaging.2012
- Sochorcova V,Proks P,Cermakova E,Knotek Z.Contrast-enhanced computed tomography of the liver, gall bladder and urogenital tract in female red-eared terrapins (Trachemys scripta elegans).Vet Med – Czech, 2017, 62(12):674-680
- Smith CR et al.Bone Scintigraphy and Computed Tomography: Advanced Diagnostic Imaging Techniques in Endangered Sea Turtles.IAAAM.2000