はじめに
現代の獣医療において、ウサギは犬および猫に次ぐ主要な伴侶動物としての地位を確立していますが、その普及に伴い、不妊手術を受けていない雌ウサギにおける生殖器疾患の発生が臨床現場での大きな課題となっています。ウサギの生殖器系は多産を実現するために高度に特化しており、その解剖学的および生理学的特性が、特有の疾患パターンの背景となっています。メスのウサギの診療において最も留意すべき点は、加齢に伴う疾患発生率の極めて高い上昇です。特に子宮腺癌は、未避妊のメスのウサギにおいて避けることのできない老化に伴う終着点とも評されるほど一般的であり、3~4歳を超える個体では、その半数以上が何らかの子宮病変を有していると推測されます。
解剖と生理
ウサギの雌性生殖器は、他の一般的な伴侶動物とは異なるいくつかの重要な特徴を持っています。これらの理解は、疾患の病態把握および外科的介入において不可欠です。
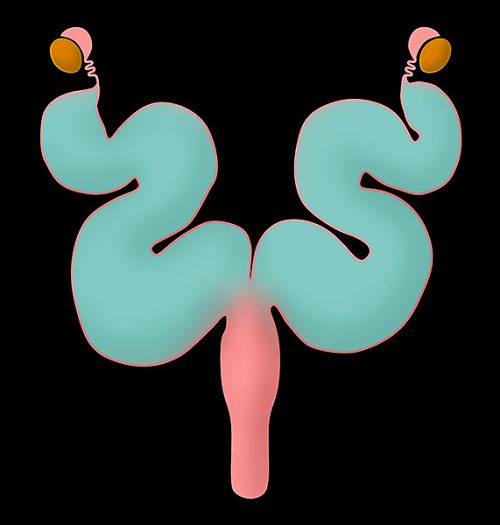
重複子宮
ウサギは重複子宮を持ち、左右の子宮角がそれぞれ独立して存在し、それぞれが独立した子宮頚管へと繋がっています。
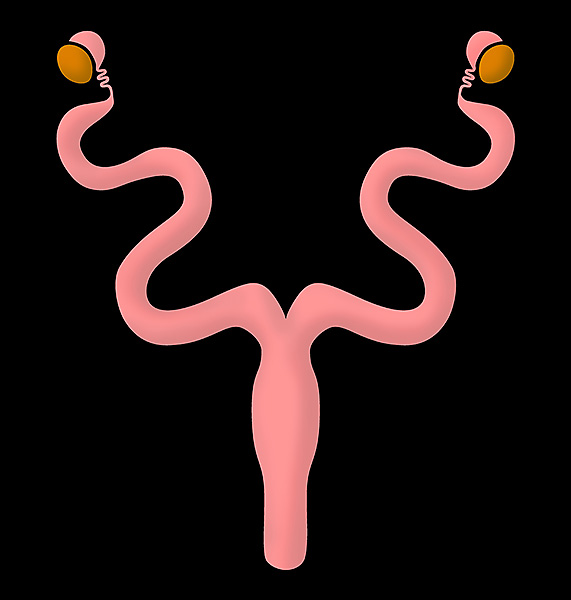
すなわち、ウサギには2つの子宮頚管が存在し、これらが膣へと開口しています 。それぞれの子宮の先に卵管と楕円形の卵巣があります。外科的な避妊手術(卵巣子宮全摘出術)を実施する際には、これら2つの頚管を確実に処置することが、残存組織によるトラブルを防ぐために極めて重要です。
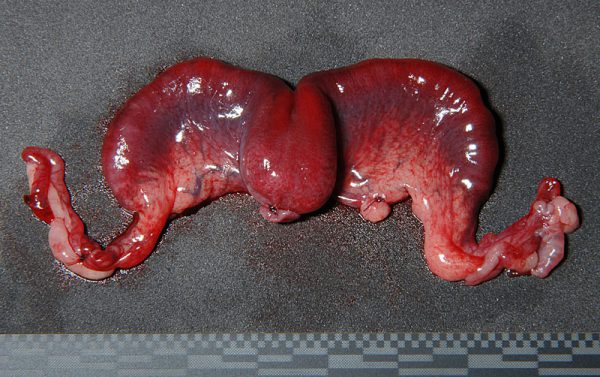
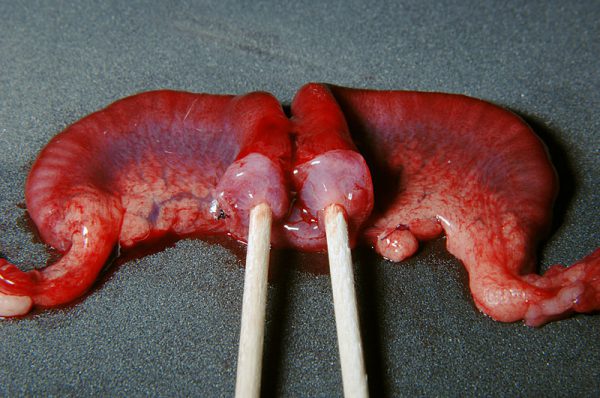
広間膜脂肪
成熟したメスのウサギの大きな特徴の一つに、子宮を支持する広間膜が顕著な脂肪貯蔵部位となることが挙げられます。特に肥満傾向にある個体や高齢個体では、子宮および卵巣の血管が大量の脂肪組織に埋没しており、手術時の血管同定および結紮を困難にする要因となります 。この脂肪組織は非常に脆弱であり、不適切な操作は容易に出血を招くため、術前の体重管理と術中の繊細な手技が要求されます。
繁殖生理
性成熟に達するのはオス7~8ヵ月齢、メス4~12ヵ月齢(小型種 4-5ヵ月齢 中型種 4-8ヵ月齢 大型種9-12ヵ月齢になります〔橋爪 1992〕。メスは成体の体の大きさの70~80%のサイズに達すると繁殖可能になるので、小型種では早く、大型種では時間がかかります。メスのウサギは犬や猫のような定期的に発情が訪れる動物でなく、12~14日間の発情期が繰り返し起こり〔星ら 1996〕、発情をしていない期間が極端に短いため、常に発情している感じになります。子宮が発情している期間が多いと、細胞変性もしやすいことから、疾病が多発する理由かもしろません。
交尾排卵
ウサギは交尾排卵動物で、交尾刺激によってLH(黄体形成ホルモン)が分泌され排卵が起こります。しかし、実際には交尾がなくても、他の個体との接触や不適切な環境刺激によって排卵が誘発されることがあり、これが偽妊娠の原因となります。偽妊娠状態では、黄体が維持されプロジェステロンが継続的に分泌されるため、子宮内膜が肥厚し、後の過形成や腫瘍化の素因となる可能性が指摘されています。
子宮腺癌
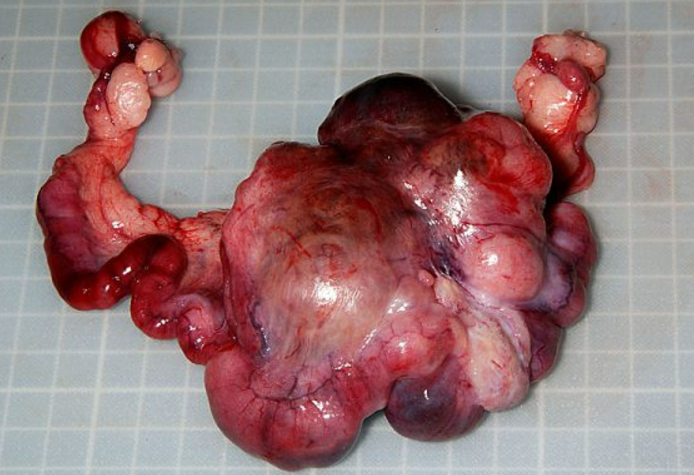
子宮腺癌(Uterine Adenocarcinoma)はメスのウサギにおいて最も発生頻度の高い腫瘍性疾患です。ウサギの子宮内膜腺由来の悪性上皮性腫瘍であり、全子宮腫瘍の大部分を占めます。この腫瘍は進行が比較的緩徐であるものの、最終的には局所浸潤および遠隔転移を引き起こし、致命的な経過をたどります。腫瘍が成熟すると、中心部に広範な凝固壊死や石灰化が生じることがあり、これが画像検査での特徴的な所見に寄与します。その発生は加齢と密接に関連しています。子宮腺癌の最大のリスク要因は年齢です。多くの臨床統計において、3歳を過ぎたあたりから発生率が急増することが示されています。
| 年齢 | 発生率 | 備考 |
| 2〜3歳 | 約4.2% | 初期発生が見られ始める時期 |
| 4歳以上 | 50〜60% | 未避妊個体の半数以上が罹患 |
| 5〜6歳 | 79.1〜80% | 老齢ウサギにおける圧倒的リスク |
歴史的なGreeneの研究によれば、5~8歳のコロニーにおける発生率は79.1%に達しており、これはウサギが十分に長生きすれば、ほぼ例外なくこの疾患に直面することを示唆しています 。一方で、2歳以下の若齢個体での発生は稀ですが、2歳での診断例も報告されており、若齢であっても臨床症状がある場合は除外できません〔Greene 1968〕 。日本国内の専門病院における898頭を対象とした大規模な遡及的研究(2006年-2020年)によれば、死亡時の年齢中央値は7歳に達しており、5歳以上の中高齢個体における最大の死因は腫瘍であることが示されています〔Shiga et al.2022〕。子宮腺癌の発生も加齢と強く相関しており、特定の年齢を境にリスクが急激に上昇することが多くの研究で裏付けられており、特に3歳および5歳という年齢は、臨床的なリスク管理において重要な閾値とされています〔Mäkitaipale et al.2022〕。
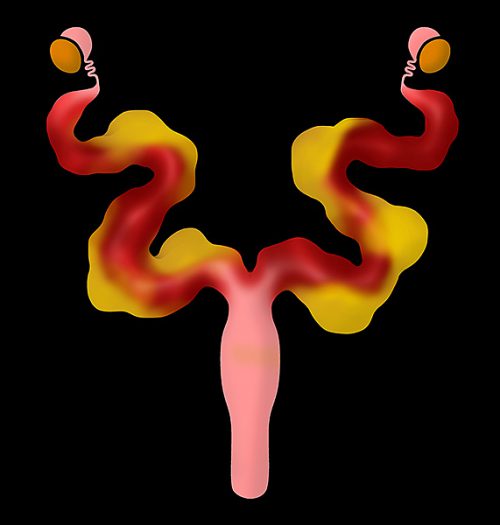
| 年齢 | 発生率 |
| 1~3歳(若齢) | 発生率は極めて低く、約4%程度と推定される |
| 3歳以上 | 3歳未満と比較して、悪性子宮腫瘍の発生リスクは約19.3倍に急増する |
| 4歳以上 | 発生率が60%に達すると報告される臨床的な転換期 |
| 5歳以上 | 未避妊個体における発生率は50~80%に達し、ピークを迎える |
| 6歳超 | 腫瘍全体の有病率が47.2%に達し、その大半が子宮腺癌 |
フィンランドの2022年発表での調査は、3歳という年齢がリスクの明確な境界線であることが示されました。この研究によれば、3歳以上のウサギにおける悪性子宮の腫瘍の有病率は40%に達したのに対し、3歳未満ではわずか5.3%でした〔Mäkitaipale et al.2022〕。この約19倍というオッズ比の増大は、ウサギの子宮内膜が3歳を過ぎる頃から生理的な老化プロセスに入り、癌抑制メカニズムの減退や、長期にわたるエストロゲン曝露の影響が顕在化することを示唆しています。

地域別の最新発生率
近年の国際的な研究は、地域や個体群によって発生率にばらつきがあることを示しつつも、一貫して年齢を最大の危険因子として特定しています。タイにおける調査(2018~22年)では、 病院に持ち込まれたウサギの生検・剖検サンプル93例のうち63例(67.74%)が腫瘍でした。その中で生殖器系の腫瘍は65.08%を占め、5歳以上のウサギはそれ以下の年齢層に比べ、生殖器腫瘍を発症する確率が3.85倍高かったです〔PORNSUKAROM et al.2023〕。香港における調査(2019~22年)では、243頭のペットウサギを対象とした遡及的研究で、子宮腺癌が全腫瘍の26.4%を占め、最も頻度の高い腫瘍でした。罹患個体の平均年齢は5.9歳、年齢範囲は2歳から10歳に及びました〔Hill et al.2024〕。北米および欧州の知見では、伝統的な文献は依然として5歳以上で80%という高い数値を支持しており、これが予防的避妊手術の強力な根拠となっています〔Van Zeeland 2017〕 。
歴史的80%数値の再評価
「未避妊の雌ウサギは5歳までに80%が子宮癌になる」という言説は、獣医学の教科書や啓発サイトにおいて長らく定説とされてきました。しかし、近年のエビデンスでは、この数値の一般化に対して慎重な見解が示されています。イギリスの獣医師マーティン・ホワイトヘッドは、この80%という数値の根拠となった1930年代から1960年代の米国の研究論文を精査し、現代のペットウサギにそのまま適用することの危うさを指摘しました。当時の研究対象は高度にインブリードされた実験用ウサギのコロニーであり、特定の血統(系統)において極端に高い発生率が記録されていました。飼育形態、餌(高カロリーなペレット中心から牧草中心へ)、およびホルモン環境が現代のペットとは大きく異なります。ホワイトヘッド自身の診療データやデンマークの小規模研究では、子宮腺癌の臨床的な遭遇頻度は、他の疾患(歯科疾患、消化管停滞、蝿蛆症など)に比べて著しく低いことが示されています。ホワイトヘッドは、5歳以上の未避妊雌において臨床的に検出可能な腫瘍がある割合は10〜13%程度と報告しています〔Whitehea 2017〕。これに対し、避妊手術を推奨する側の専門家は、たとえ80%という数字が歴史的なバイアスを含んでいたとしても、本疾患が稀ではないことは事実であり、かつ致死率が高いことを強調しています。特に注目すべきは、フィンランドの研究で見られた疾患が疑われていないグループにおける知見です。子宮疾患の臨床徴候がない状態で避妊手術や剖検を受けたウサギのうち、3歳以上の個体の29%に組織学的な新生物(腺癌、腺腫、上皮内癌)が認められました。このことは、多くのウサギが臨床的な症状が出る前の潜在的な癌を抱えたまま高齢期を過ごしている可能性を示しており、マクロな視点(触診や身体検査)だけでは発生率を過小評価してしまうリスクを示唆しています〔Mäkitaipale et al.2022〕。
病理学的検索
ウサギの子宮腺癌は、多くの場合、正常な子宮内膜から突然発生するのではなく、一連の増殖性変化を経て進行する連続体としての側面を持っており、子宮腺癌は、内膜ポリープ形成→嚢胞状増殖→腺腫状増殖→腺癌というステージを経て進行すると考えられています。組織学的には、内膜上皮細胞の脱分化、異形成、未分化が特徴であり、正常な細胞が持つ繊毛や分泌顆粒が消失していきます。つまり、病理学的に過形成、嚢胞状、そして腺腫状に増殖し、腺上皮が内腔に向かって乳頭状に増殖し、まずは子宮内膜症と呼ばれる病態を呈します。
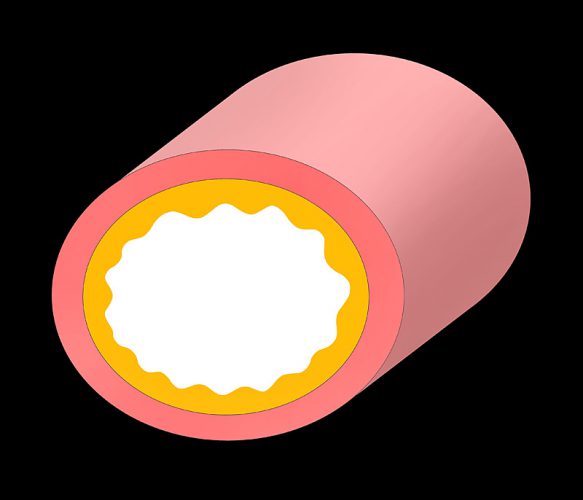
嚢胞状子宮内膜過形成は非腫瘍性の病変ですが、子宮腺癌を伴う症例の85%で併発しており、加齢に伴いその頻度は上昇します。1歳という若齢でも報告がありますが、加齢に伴うコラーゲン沈着の増加が、この増殖性病変から腫瘍への転換を促進すると考えられています〔Klaphake et al.2012,Campbell-Ward et al.2010,Vinci et al.2010,Asakawa et al.2008〕。
子宮腺癌の組織学的亜型
子宮腺癌は組織学的に大きく2つのパターンに分類され、それぞれ生物学的挙動が異なります〔Vaccaro et al.2024〕。
乳頭状腺癌 (Papillary Adenocarcinoma): 腺腔内に複雑な乳頭状の突起を形成します。この型は比較的早期にエストロゲン受容体(ER-α)およびプロゲステロン受容体(PR)の発現を消失する傾向があり、ホルモン依存性から自律的な増殖へと移行しやすいです 。
管状/充実性腺癌 (Tubular/Solid Adenocarcinoma): 腺管構造や細胞の充実性集塊が筋層を置換するように浸潤します。
また、最新の研究では、ウサギの子宮腺癌においてシクロオキシゲナーゼ-2(COX-2)が高度に発現していることが確認されました。COX-2の過剰発現は腫瘍の血管新生や浸潤を促進するため、COX-2阻害薬(メロキシカム等)が補助的な治療として生存期間を延長させる可能性が示唆されています〔Vaccaro et al.2024〕 。
嚢胞状子宮内膜過形成
嚢胞状子宮内膜過形成(Cystic Endometrial Hyperplasia: CEH)は非腫瘍性の子宮病変として最も一般的です。プロジェステロンの持続的な刺激により、子宮内膜の腺組織が嚢胞状に肥大・増殖します。平均発症年齢は約4.5歳で、腺癌よりも若齢から見られる傾向があります。腺癌の前段階と考えられていますが、腺癌を伴わない独立した症例も多数存在します 。出血および貧血などか見られ、子宮腺癌と区別が困難です。
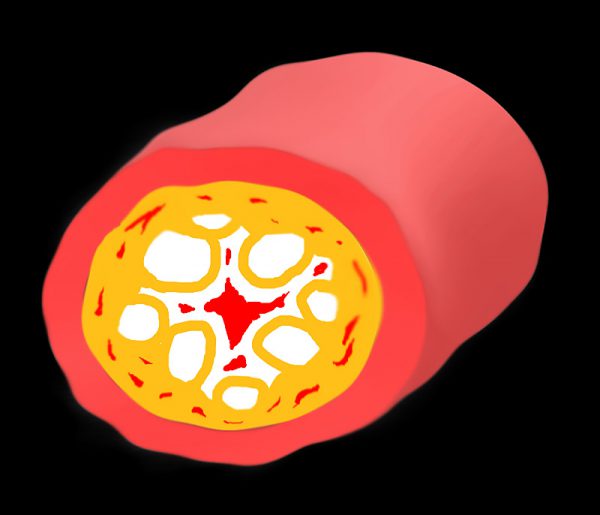
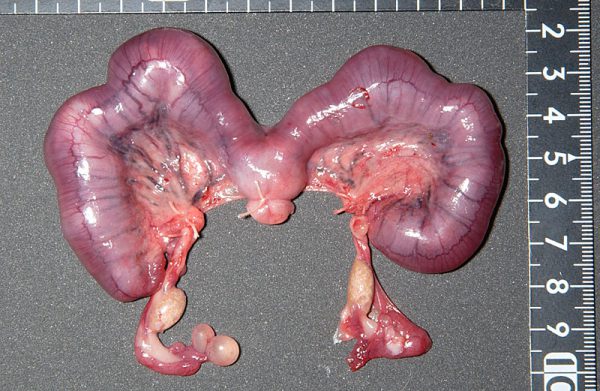
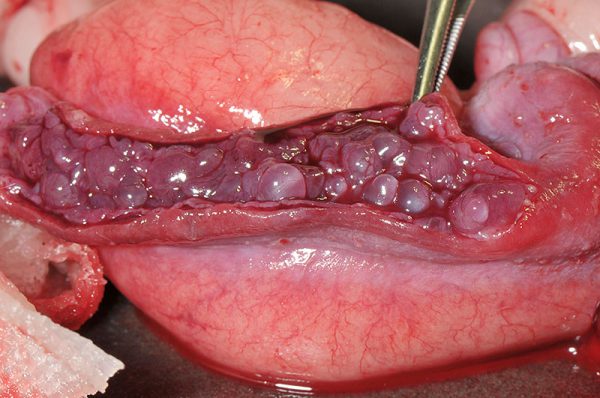
子宮内膜静脈瘤
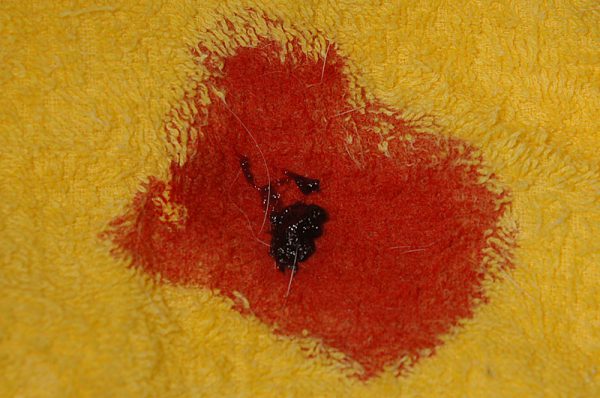
子宮内膜静脈瘤(Endometrial Venous Aneurysms)はウサギに特有の疾患で、子宮内膜の静脈が異常に拡張し、それが定期的に破裂して子宮腔内へ出血します。型取りされたような円柱状の血餅が尿とともに排出されます。突然の大量出血により、死亡するリスクもあります。
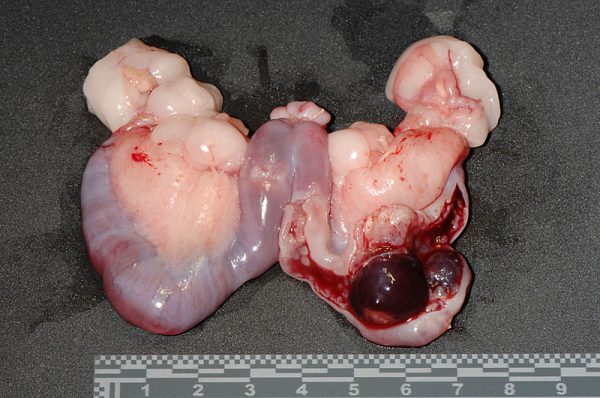
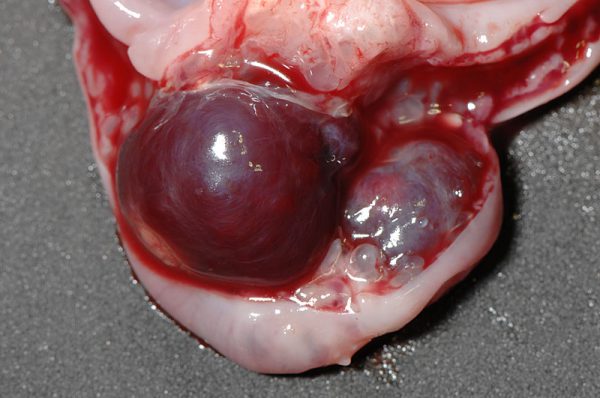
子宮水腫/子宮粘液症
子宮水腫(Hydrometra)は子宮腔内に無菌性の漿液(水腫)、子宮粘液症(Mucometra)は粘液が大量に蓄積する病態です。著明な腹部膨満を示し、蓄積した液体が横隔膜を圧迫し、呼吸数を増加させたり、胃の拡張を制限して食欲不振を引き起こしたりします。超音波にて子宮の著明な拡張と内部の無エコー〜低エコー液体を確認します。
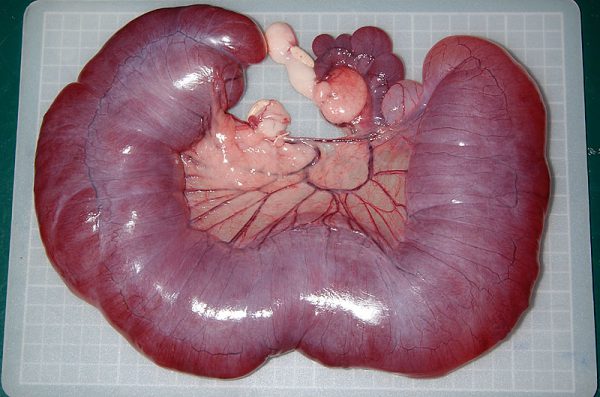
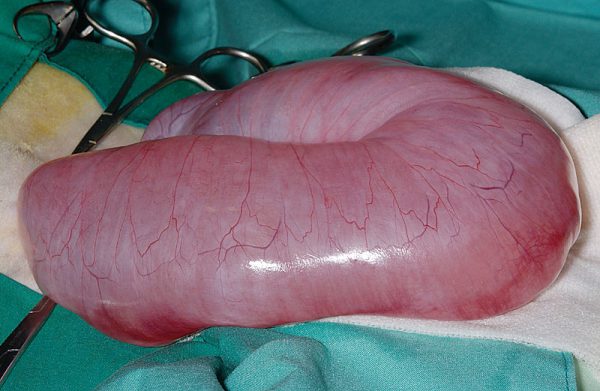
ウサギが腹囲膨大を示し、太ったなと思っていたら、子宮水腫であったというケースが多いです。子宮水腫では陰部からの出血は多くないので、発見が遅れがちになります。


子宮蓄膿症・感染性内膜炎
子宮蓄膿症(Pyometra)は、子宮内に細菌感染が生じ、膿が蓄積する緊急疾患です。不衛生な飼育環境、交尾による感染、あるいは自己の鼻腔(スナッフル)などからの感染が主なルートです。Pasteurella multocida、Staphylococcus aureusなどか分離されます。加齢や偽妊娠に伴うCEHがベースとなり、プロジェステロンによる子宮頚管の閉鎖と局所免疫の低下が重なることで、細菌が爆発的に増殖します。
その他の子宮腫瘍
子宮壁の平滑筋層から発生する間葉系腫瘍も、上皮性腫瘍に次いで重要です。これらは平滑筋腫、平滑筋肉腫、およびその他の稀な軟部組織腫瘍に分類されます 。ウサギの子宮では、上皮系や平滑筋由来以外の稀な腫瘍も散発的に報告されています 。
子宮平滑筋腫(Uterine Leiomyoma)
平滑筋腫は、子宮筋層を構成する平滑筋細胞由来の良性腫瘍です。ウサギにおいて、これは子宮腺癌、平滑筋肉腫に次いで頻度の高い腫瘍であり、ある研究では子宮病変の約 9% 程度を占めると報告されています。多くの場合、定期検診や他の疾患での手術時に偶然発見されます。良性であるため転移の心配はありませんが、巨大化して腹部を圧迫したり、子宮腺癌と併発したりすることがあります 。
子宮平滑筋肉腫(Uterine Leiomyosarcoma)
平滑筋肉腫は、平滑筋由来の悪性腫瘍であり、侵襲的な増殖と早期の血行性転移を特徴とします。平滑筋腫とは異なり、早期に肺や腹腔内臓器へ転移する傾向があり、予後は腺癌よりも慎重に判断される必要があります。
子宮血管肉腫(Uterine Hemangiosarcoma)
血管内皮細胞由来の悪性腫瘍であり、ウサギでは極めて稀な例として報告されています。臨床的特徴: 腫瘍細胞は CD31 陽性を示し、急速に進行して腹腔内出血を引き起こす可能性があります 。
悪性混合ミュラー管腫瘍(Malignant Mixed Müllerian Tumor)
癌腫 (上皮成分) と肉腫 (間葉成分) の両方が混在する、極めて侵襲性の高い悪性腫瘍です 。診断時にはすでに広範な転移を伴っていることが多く、肺、縦隔、横隔膜、リンパ節などへの播種が報告されています 。非常に予後が悪い疾患の一つです。
絨毛癌(Choriocarcinoma)・テラトーマ(Teratoma)
絨毛癌は胎盤組織由来の腫瘍であり、ウサギでの報告は極めて稀です 。テラトーマは多分化能を持つ細胞由来の腫瘍で、軟骨、骨、毛髪、上皮などの様々な組織成分を含みます。卵巣に発生することが多いですが、稀に子宮での報告もあります。
卵巣疾患
卵巣疾患は子宮疾患に隠れて見落とされがちですが、不妊や全身症状の原因となります〔BERTRAM et al.2017〕 。
卵巣嚢胞
ウサギにおける卵巣嚢胞(Ovarian Cysts)は、ホルモンバランスの乱れや偽妊娠と関連しています 。卵胞嚢胞(Follicular Cysts)は 卵巣皮質に形成される単一または複数の嚢胞です。発症平均年齢は26ヵ月齢と報告があります〔BERTRAM et al.2017〕。エストロゲン分泌を継続させ、子宮内膜の変性を促進する要因となります。網状卵巣嚢胞(Cystic Rete Ovarii)は 卵巣門付近から発生する嚢胞で、高齢個体(中央値87ヵ月)に見られます。時に非常に巨大化(5cm以上)し、腹腔内臓器を圧迫します〔BERTRAM et al.2017〕 。
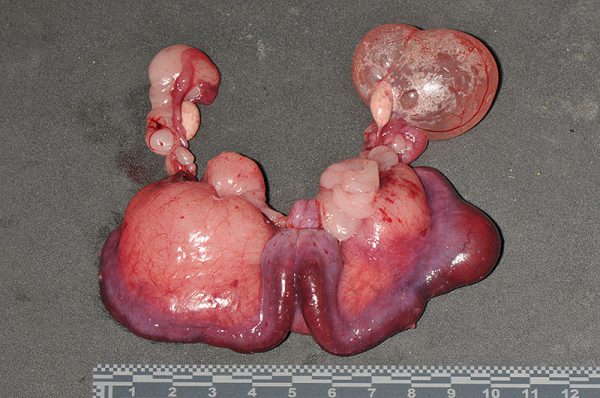
卵巣腫瘍
ウサギでは卵巣腫瘍(Ovarian Neoplasia)は比較的稀ですが、高齢個体や子宮疾患を持つ個体で偶発的に発見されることがあります。顆粒膜細胞腫(Granulosa Cell Tumor)が最も代表的な卵巣腫瘍です 。エストロゲンやプロジェステロンを産生し、子宮疾患や不妊を引き起こします。組織学的にはCall-Exner体という特徴的な所見を呈することがあります。上皮由来の腫瘍である卵巣腺腫・腺癌も稀に発生します。その他、血管腫、平滑筋腫、未分類の軟部組織腫瘍などが報告されています〔BERTRAM et al.2017〕。
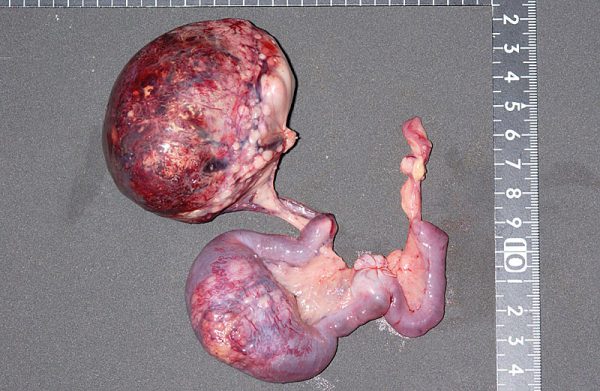
子宮腺癌の発生環境
品種
年齢が最大の決定要因である一方、遺伝的背景(品種)も無視できない要因である。歴史的な実験データと現代のペット個体群のデータの双方から、品種ごとのリスク傾向を抽出できます。タン(Tan)、フレンチ・シルバー(French Silver)、ハバナ(Havana)、ダッチ(Dutch) 。特にタン種では、50%を超える発生率が報告されることもあります。ニュージーランド・ホワイト(New Zealand White)、ポーリッシュ(Polish)、ヒマラヤン(Himalayan)などは、相対的に発生が遅い、あるいは低い傾向にあるとされていますが、依然として高齢では高リスクです。これらの品種では、特定の遺伝子座における癌抑制遺伝子の欠如や、エストロゲンに対する標的組織の感受性の高さが推測されています 。一方、近年人気のネザーランド・ドワーフやホーランド・ロップといった小型種においても発症は一般的です。ただし、フィンランドの研究においても統計学的な有意差(P=0.249)までは認められておらず、品種によるリスクの差は、個体群内での近交係数や系統維持の歴史に依存する部分が大きいと考えられる 。現代のペットにおいては、品種よりも「避妊されていない状態での加齢」そのものが圧倒的なリスク因子であるという見解が一般的になっています〔Mäkitaipale et al.2022〕。。
繁殖歴
重要な臨床的知見として、子宮腺癌の発生は「繁殖の有無(出産の経験)」とは無関係であることが証明されています 。以前は「出産を経験させれば癌にならない」という俗説がありましたが、学術的には否定されており、繁殖に使用されている優秀な母ウサギであっても、加齢とともに等しく癌のリスクに晒されます 。
内分泌と子宮疾患と乳腺腫瘍
ウサギの生殖生理は「交尾排卵型」であり、これは定期的な発情周期(黄体期)を持たないことを意味します。しかし、刺激による排卵が頻繁に起こる環境や、偽妊娠が繰り返される環境下では、子宮内膜は非常に不安定なホルモン動態に曝されることになります 。
エストロゲンの強力な増殖作用
エストロゲンは、子宮内膜の増殖と分化を制御する中心的なホルモンです。ウサギの子宮腺癌の主要な仮説の一つは、「拮抗されないエストロゲン刺激です 。これは、プロゲステロンによる抑制効果が不十分な状態で、エストロゲンが長期にわたり作用し続けることが細胞の悪性変換を誘発するという考え方です。エストロゲン受容体(ER-α)の表現型解析によれば、正常な子宮内膜や増生組織の多くでER-αが陽性を示します 。しかし、腺癌の進行に伴い受容体の発現パターンには変化が生じます〔Kim et al.2025〕。
| 組織型 | ER‐α?PR発現の特徴 | 臨床的意義 |
| 正常内膜・増生組織 | 高い発現維持 | ホルモン感受性が維持されている |
| 管状/充実性腺癌 | 発現を維持する傾向 | 早期から筋層浸潤を示すが、受容体は陽性 |
| 乳頭状腺癌 | 早期に発現を消失 | ホルモン依存性を失い、より自律的な増殖を示す |
プロゲステロンと偽妊娠の影響
プロゲステロンは排卵後の黄体から分泌されます。ウサギでは、不妊交尾や他のウサギとの接触、あるいは特定の刺激により「偽妊娠」が引き起こされます。この期間(通常15〜18日間)、血中プロゲステロン濃度は高く維持され、子宮内膜の腺分泌を活性化させます 。プロゲステロンの作用により子宮頸管が機能的に閉鎖し、子宮内に分泌液が蓄積することで、子宮水腫(hydrometra)や粘液症、あるいは子宮内膜増生のリスクが高まります〔Hristov et al.2017〕 。免疫組織化学的所見からは、プロゲステロンが直接的に発癌を誘導しているという証拠は限定的ですが、エストロゲンとの相乗効果や受容体濃度の変調を通じて、腫瘍発生の環境を整えている可能性が示唆されています 。
プロラクチン(催乳ホルモン)
近年の研究で最も注目されているのがプロラクチンの役割です。プロラクチンは単に乳汁分泌を促すだけでなく、子宮組織におけるステロイド受容体の感受性を調節するモジュレーターとして機能しています〔Daniel et al.1988〕。プロラクチンは子宮内膜におけるエストロゲン受容体およびプロゲステロン受容体の濃度を上昇させることが研究で示されています。これにより、子宮のエストロゲンに対する応答性が異常に強化される可能性があります。子宮腺癌細胞自体がプロラクチン受容体(PRL-R)を発現しており、局所的に分泌されるプロラクチンが細胞増殖シグナル(Jak-STAT経路、Ras/MAPK経路、PI3K経路)を活性化し、癌の進行を促進するという機構が考えられています〔Daniel et al.1988〕。 新生児期や成長期における子宮腺の形成にもプロラクチンが関与しており、このホルモンの過剰な曝露が将来的な腺組織の異形成に繋がると推測されています 。
子宮腺癌と乳腺腫瘍
臨床現場において、子宮腺癌と乳腺腫瘍が同時に発見されることは極めて一般的です。これは単なる偶発的な一致ではなく、全身的なホルモン環境の不均衡が両器官に同時に作用していることを示唆しています。大規模な回顧的研究および複数の臨床報告から、両疾患の併発率は極めて高いことが裏付けられています〔Kim et al.2025〕。乳腺と子宮の両方に作用する共通の因子として、プロラクチンが最有力候補です。ウサギの乳腺腫瘍の多くは、組織学的に「分泌活性(乳汁様物質の産生)」を有しており、これは強力なプロラクチン刺激の存在を示唆しています〔Schöniger et al.2019〕 。特筆すべきは、プロラクチン分泌性の下垂体腺腫を伴うウサギの症例報告です。この症例では、著しい高プロラクチン血症により、重度の乳腺嚢胞、異形成、および乳腺腺癌が誘発されていました 。また、免疫抑制剤のシクロスポリン投与が副作用としてプロラクチン値を上昇させ、その結果として乳腺増生を引き起こしたという実験データも存在します 。これらの知見は、プロラクチン軸の異常が「子宮疾患+乳腺疾患」という併発パターンを生む主要な駆動源であることを示しています〔Schöniger et al.2019〕 。
卵巣・子宮除去による乳腺腫瘍の予防効果
「卵巣を除去すれば乳腺腫瘍は予防できるのか」という問いに対し、獣医学的な回答は「時期を選べば極めて高い効果があるが、高齢になってからでは限定的である」となります。乳腺組織は、思春期以降の卵巣から分泌される性ステロイド(エストロゲン、プロゲステロン)の累積的な刺激によって細胞変異のリスクが高まります。卵巣を摘出することは、これらの「増殖のガソリン」を遮断することを意味します。つまり、早期実施(性成熟直後)といわれる4~6ヵ月齢での避妊手術は、乳腺組織が本格的なホルモン刺激を受ける前に介入するため、乳腺腫瘍の発生をほぼ完全に、あるいは極めて高い確率で抑制できると考えられています。既に3~4歳を超えた未避妊個体では、既に乳腺組織において「前癌状態(前新生物性病変)」が形成されている可能性があります。この段階で卵巣を除去しても、既に自律的な増殖能を得た細胞を止めることは難しく、将来的な乳腺腫瘍の発症を完全には防げない場合があります〔Settai et al.2020〕 。ただし、子宮腺癌を100%予防できるという点だけでも、高齢個体で手術を行う医学的な意義は依然として極めて高いと言えます。
症状
子宮疾患の初期段階では、ウサギは全く無症状で、あるいは極めて軽微な変化しか示しません。 多くの場合、疾患が進行し、二次的な合併症が生じてから顕在化します。
繁殖個体における初期兆候
繁殖に供されているメのスウサギでは、繁殖成績の低下が観察されます。受胎率の低下および不妊、産子数の減少、胎児の吸収、流産、または死産の増加 、出産後の育児放棄や食子、胎児停滞や難産などです 。
一般的な臨床徴候
非繁殖個体、あるいは進行した症例で見られる主要な症状は以下の通りです。
出血性分泌物
最も代表的な症状は出血性分泌物です。実際には尿路疾患ではなく、子宮からの出血が排尿時に混入するもので、血尿が断続的に発生します。

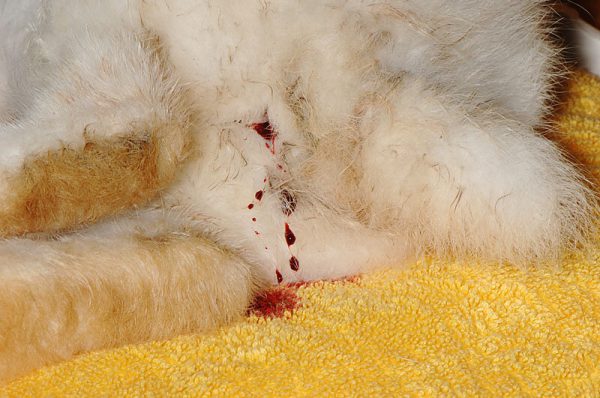
尿の終わりに鮮血が混じる、あるいは尿の中に独立した血のスポットや血餅が見られます 。これは実際には血尿(膀胱や腎臓からの出血)ではなく、子宮からの出血が排尿時に排出されている状態です。
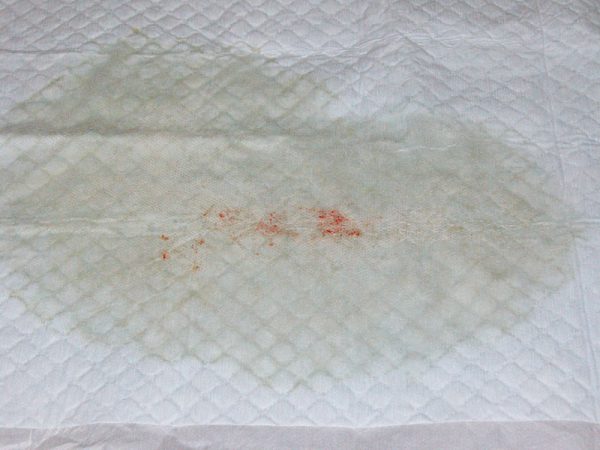
また、 漿液血性の分泌物が観察されることがあります。

腹部腫瘤と膨満
子宮腺癌あるいは子宮水腫などが進行した症例では、下腹部に硬く不規則な腫瘤が触知されます 。これは腫大した子宮角そのものであり、しばしば左右非対称な膨らみとして認識されます。
乳腺の異常
子宮腫瘍に伴うホルモンバランスの変化により、乳腺の腫脹、囊胞形成、あるいは透明から乳白色の分泌物が認められることがあります。これは子宮疾患を有する個体の約30%前後で併発すると報告されています 。
全身状態の悪化
腫瘍が巨大化したり転移が進んだりすると、食欲不振、元気消失、活動低下、慢性的な体重減少が現れます 。また、持続的な出血による重度の貧血が生じると、可視粘膜の蒼白や虚脱が見られます 。
呼吸器症状
肺転移が成立した場合、努力性呼吸、浅快呼吸、あるいは鼻翼呼吸や開口呼吸といった呼吸困難のサインが現れます 。この段階での発見は予後が極めて不良であることを示唆します 。
行動の異常
攻撃性の増加、巣作り行動の頻発(偽妊娠に関連)などが初期に見られることがあります。
転移
子宮腺癌は、初期には子宮角の局所に留まりますが、時間の経過とともに多中心性に発生し、両側の子宮角を侵すようになります 。転移は疾患の後半段階(臨床症状の発現から12~24ヵ月後)に発生することが多いとされています。子宮漿膜を突き抜け、腹膜、膀胱、直腸、広間膜などの隣接臓器へ直接広がります(直接浸潤) 。血行性・リンパ行性転移も起こり、 最も高頻度に転移が認められる臓器は肺です 。その他、肝臓、脾臓、腎臓、副腎、リンパ節、脳、骨、皮膚など、多岐にわたる遠隔転移します。巨大化した腫瘍が破綻し、腹腔内への出血や、腫瘍細胞の散布に伴う癌性腹膜炎、あるいは敗血症性腹膜炎を引き起こすこともあります。
診断・検査
子宮の病気はレントゲン検査やエコー検査で判断します。明確でない時や腫瘍の転移の詳細はCT検査をします。出血がひどい時には血液検査で貧血の有無などを確認します。腫瘍か腫瘍ではないのか?一番知りたい所だと思いますが、確定するには、外科手術で摘出した子宮を病理検査で調べるしか方法はありません。レントゲンやエコーである程度の大きさの子宮の腫瘍がある、CT検査で転移があるなどの情報から、悪性腫瘍の可能性が高いということは言えるかもしれません。
身体検査と触診
尾側腹部の慎重な触診により、肥厚した子宮角や、結節状の腫瘤を確認します 。正常な子宮は非常に細く触知困難ですが、腺癌や過形成がある場合は容易に感知できます。ただし、妊娠や子宮蓄膿症との判別、および子宮壁の脆弱性を考慮し、過度な圧迫は避けるべきです 。
血液検査(CBC・生化学)
貧血の評価として赤血球数、ヘモグロビン、ヘマトクリットの低下を確認します。慢性的な失血による再生性または非再生性貧血が一般的です 。 BUN、アルブミン、肝酵素の測定により、全身状態の把握と麻酔リスクの評価を行います 。
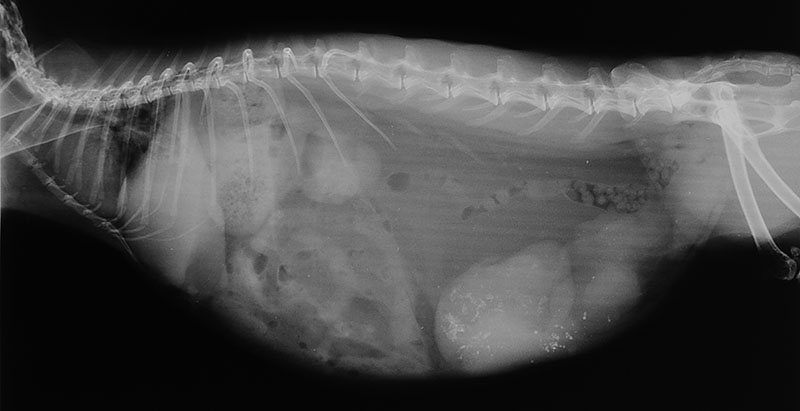
X線検査
下腹部に軟部組織密度の腫瘤像や、拡大した管状の子宮角を確認できます。ウサギの子宮腺癌において特に特徴的なのは、子宮壁に一致して認められる点状または斑状の石灰化沈着です 。また、転移の有無を確認するために、胸部レントゲン検査は診断の全プロセスにおいて必須の項目となります。
超音波検査
超音波検査では 子宮壁の構造(厚み、不均一性)、嚢胞の有無、内腔の液体貯留(水腫、粘液症、蓄膿症)を評価するために最も感度の高い方法です。
子宮内腔の拡張:子宮内腔に液体貯留することで拡張します。
嚢胞状子宮内膜過形成:子宮陰影の中に無エコーの嚢胞構造が確認できます。
子宮腺癌:腫瘍が成熟すると、中心部に広範な凝固壊死や石灰化が生じます。
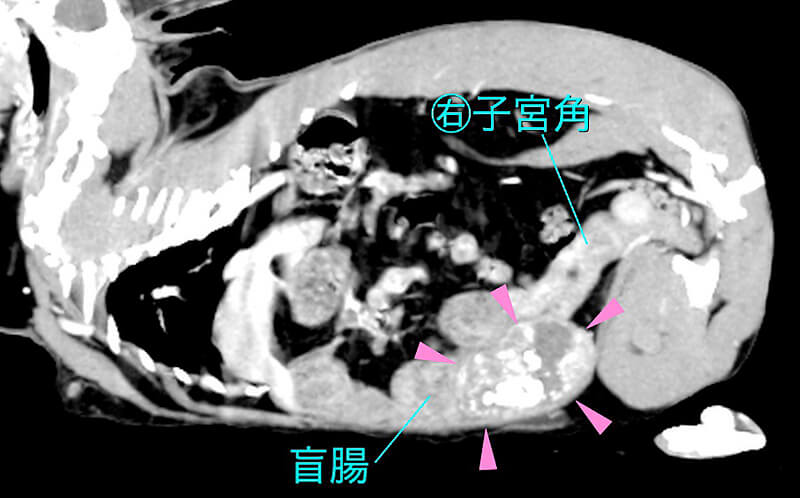
CT検査
X線検査や超音波検査で子宮が明確でない時や子宮の腫瘍の初期転移まで判断できます。
尿検査
血尿の確認(ポルフィリン尿との差別化)を行います。潜血反応陽性かつ遠心分離で赤血球が確認されれば真の血尿/膣出血と判断されます 。
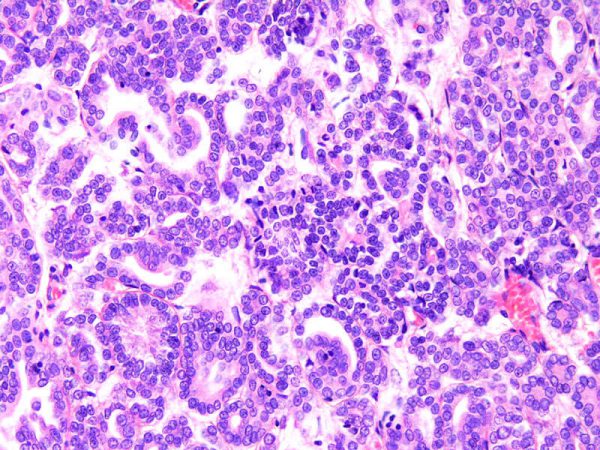
病理組織学的検査
最終的な確定診断は、摘出された組織の病理組織学的検査に基づきます。
治療
すべての雌ウサギの生殖器疾患に対する根本的な治療法は「卵巣子宮全摘出術(Ovariohysterectomy: OHE)」です 。予後は、手術の「タイミング」に決定的に左右されます 。非腫瘍性疾患(CEH、静脈瘤、水腫、蓄膿症)の場合、適切な外科処置が行われれば、予後は一般に良好であり、再発の心配もありません 。子宮腺癌は未治療の場合、一般的に6~24ヶ月以内に死亡します〔Meredith 2014〕。
【手術】ウサギの卵巣・子宮摘出手術とお薦め外科手術器具の解説はコチラ
| 病態 | 予後 | 備考 |
| 転移なし(限局性) | 良好〜極めて良好 | 手術により完治。寿命に影響なし。 |
| 局所浸潤あり | 警戒(Guarded) | 完全切除が困難な場合があり、再発リスク。 |
| 遠隔転移あり(肺等) | 不良(Poor) | 手術後の平均生存期間は12〜18ヶ月〔Kim et al.2025〕。緩和ケアが中心。 |
子宮腺癌で手術を行った個体、あるいは高齢で未避妊の個体については、身体検査および胸部X線: 術後1〜2年間は、3ヶ月から6ヶ月おきに転移の有無を確認します 。超音波検査: 定期的な腹部チェックにより、微小な転移巣や併発する乳腺病変を早期発見します 。
ホルモン治療
外科手術が不可能な症例や、転移が認められる症例において、ホルモン動態を制御する内科治療が検討されます。しかし、ウサギにおけるその効果と安全性については慎重な評価が必要です。
【治療】エキゾチックアニマルのリュープリン(GnRHアゴニスト)治療
GnRHアゴニストインプラント(デスロレリン)
デスロレリン(Suprelorin®)は、持続的なGnRH刺激を通じて下垂体を脱感作させ、性ホルモン分泌を抑制する徐放性製剤です 。利点は1回の投与で数ヶ月(約9ヶ月以上)にわたる生殖機能の抑制が可能です。オスウサギでは精巣容積の減少とテストステロンの低下が確認されており、外科手術に代わる避妊手段としての有効性が示されています 〔Schoemaker 2018〕。欠点とリスクはメスウサギにおいては深刻な懸念があります。デスロレリンを投与した若いメスウサギを追跡した研究では、過半数の個体が2歳になる前に子宮内膜炎や子宮内膜増生を発症しました〔Schoemaker 2018〕 。これは、投与初期の「フレア現象(一時的なホルモン上昇)」や、不完全な抑制による慢性的な低用量刺激が子宮の病理的変化を助長した可能性が考えられています。したがって、子宮腺癌の予防目的での使用は、現状では推奨されません。
GnRHアンタゴニスト(デガレリクス)
最新の研究では、フレア現象を伴わないGnRHアンタゴニストであるデガレリクス(Degarelix)のウサギへの適用が検討されています。デガレリクスは投与直後から迅速にLH、FSH、および性ステロイドを低下させ、その効果も強力です 。将来的に、術前の腫瘍縮小や、緩和ケアにおける標準的な選択肢となる可能性を秘めています。
抗エストロゲン薬(タモキシフェン)とアロマターゼ阻害薬
乳がん治療薬であるタモキシフェンは、ウサギの子宮において抗エストロゲン作用を示し、受容体の挙動を変化させることが確認されています 。しかし、長期的な癌抑制効果や安全性に関する臨床データは不足しており、ヒトにおいて指摘されている「逆に子宮がんを誘発する」というリスクも無視できません〔Schöniger et al.2019〕 。
新たなアプローチ:COX-2阻害薬(メロキシカム)
厳密なホルモン治療ではありませんが、ホルモン依存性腫瘍の増殖に深く関与するシクロオキシゲナーゼ-2(COX-2)を標的とした治療が注目されています。ウサギの子宮腺癌の多くでCOX-2が過剰発現しており、非ステロイド性抗炎症薬であるメロキシカムを術後に継続投与した症例では、生存期間が有意に延長したという報告があります〔Vaccaro et al.2024〕 。これは、プロスタグランジン産生を抑えることで血管新生や細胞増殖を阻害する「メトロノミック治療」に近い効果を発揮していると考えられています 。
補助的治療
現在、ウサギの子宮腺癌に対して明確な効果を示す化学療法 (抗がん剤) プロトコルは確立されていません 。放射線治療についても報告は極めて限定的です。そのため、手術が不可能な症例では、鎮痛管理や栄養サポートを中心とした緩和ケアが主軸となります 。
予防
子宮腫瘍は、早期の避妊手術によって 100% 予防することが可能な疾患です 。獣医学的な推奨として、繁殖を予定していない雌ウサギは、生後 6ヶ月から 12ヶ月齢の間に避妊手術を受けるべきです 。3歳を過ぎると子宮内膜に初期の変化が生じ始める可能性があるため、可能な限り若いうちの手術が望ましいとされています 。避妊手術は、子宮腫瘍だけでなく、静脈瘤、子宮蓄膿症、さらには乳腺腫瘍の発生リスクをも大幅に低減させる、ウサギの健康寿命を延ばすための最も効果的な予防医学的手段です 。腫瘍の発現を抑えるようなサプリメントの投与も一つの方法でしょう。
腫瘍にうちかつサプリはコレ
サプリ配合のペレットはコレ
出血が多い時のサプリメントはコレ
これがポイント!
・ウサギに子宮の病気は多い
・年中発情があるのが原因?
・赤い尿で初めて気づく
・健診ならもっと早くに発見?
・ウサギの子宮腫瘍は癌が多い
・ウサギの子宮検診受けるべき
参考文献
- Asakawa MG, Goldschmidt MH, Une Y, et al. The immunohistochemical evaluation of estrogen receptor-a and progesterone receptors of normal, hyperplastic, and neoplastic endometrium in 88 pet rabbits.Vet Pathol45(2):217-225.2008
- BERTRAM CA et al.Ovarian lesions in 44 rabbits (Oryctolagus cuniculus).J Vet Med Sci79(12):1994-1997.201
- Campbell-Ward M, Meredith A. Rabbits.In BSAVA Manual of Exotic Pets 5th ed.Meredith A, Johnson-Delaney C eds.British Small Animal Veterinary Association.Gloucester:p87-93.2010
- Daniel JC,Juneja SC,Taylor SP,Lonergan PB,Sullivan PK,Chilton BS.Variability in the response of the rabbit uterus to progesterone as influenced by prolactin.Reproduction1.1988
- Greene HSN.Adenocarcinoma of uterine fundus in the rabbit.Annals of the New York Academy of Sciences75:535-542.1968
- Hill F et al.Neoplastic and non-neoplastic lesions in biopsy samples from pet rabbits in Hong Kong:a retrospective analysis, 2019-2022.J Vet Diagn Invest36(5):701‐710.2024
- Hristov KJ et al.Case Study Of Hydrometra And Uterine Adenocarcinoma In A Pet Rabbit.Journal of Medical and Dental Practice 4(1):544-550.2017
- Kim S et al.A case of uterine adenocarcinoma in companion rabbit.Journal of the Preventive Veterinary Medicine Vol.49 No.4 pp.274-276.2025
- Klaphake E,Paul-Murphy J.Disorders of the reproductive and urinary systems.In Ferrets, Rabbits,. and Rodents:Clinical Medicine and Surgery 3rd ed.Quesenberry K,Carpenter J edsSt.Louis: Elsevier:p218-219.2012
- Shiga T et al.Age at death and cause of death of pet rabbits (Oryctolagus cuniculus) seen at
an exotic animal clinic in Tokyo, Japan: a retrospective study of 898 cases.Journal of Exotic Pet Medicine43.2022 - Schöniger S et al.A Review on Mammary Tumors in Rabbits: Translation of Pathology into Medical Care.Animals (Basel);9(10):762.2019
- Settai K et al.Assessment of reported uterine lesions diagnosed histologically after ovariohysterectomy in 1,928 pet rabbits (Oryctolagus cuniculus).J Am Vet Med Assoc;257(10):1045-1050.2020
- Mäkitaipale J et al.Prospective survey of neoplastic and non-neoplastic uterine disorders in 116 domestic rabbits (Oryctolagus cuniculus).Journal of Exotic Pet Medicine41.2022
- Mäkitaipale J,Airas N,Engblom S,Linden J.Prospective survey of neoplastic and non-neoplastic uterine disorders in 116 domestic rabbits(Oryctolagus cuniculus),Journal of Exotic Pet Medicine41:p3-8.2022
- Meredith A,Lord B.In BSAVA Manual of rabbit medicine.Meredith A. Lord B.eds.British Small Animal Veterinary Association.Gloucester, :p191-204.2014
- PORNSUKAROM S et al.Analysis of occurrence and risk factors associated with pet rabbits’ tumors in Central Thailand.J Vet Med Sci85(12):1341-1347.2023
- Schöniger S et al.A Review on Mammary Tumors in Rabbits: Translation of Pathology into Medical Care.Animals (Basel)9(10):762.2019
- Schoemaker NJ.Gonadotrophin-Releasing Hormone Agonists and Other Contraceptive Medications in Exotic Companion Animals.Vet Clin Exot Anim21:443‐464.2018
- Van Zeeland Y.Rabbit Oncology:Diseases,Diagnostics, and Therapeutics.Vet Clin N Am Exot Anim Pract20:135-182.2017
- Vaccaro E et al.Immunohistochemical Investigation of Cyclooxygenase-2 Expression in Rabbit Uterine Adenocarcinoma and the Potential Use of COX-2 Inhibitors in Cancer Therapy.Animals (Basel)14(22):3169.2024
- Vinci A,Bacci B,Benazzi C et al.Progesterone receptor expression and proliferative activity in uterine tumors of pet rabbits. J Comp Pathol142(4):323–327.2010
- Whitehea ML.Neutering of pet rabbits.Veterinary Record180(8):204.1-205.2017
- 星修三,山内亮.家畜臨床繁殖学 (改訂新版).朝倉書店.東京.1990





